Kenaikan titik didih adalah selisih titik didih larutan dengan pelarutnya pada tekanan konstan, sedangkan penurunan titik beku adalah selisih titik beku larutan dengan pelarutnya pada tekanan konstan. Contoh soal sifat koligatif larutan kenaikan titik didih dan penurunan titik beku adalah sebagai berikut:
Contoh Soal Sifat Koligatif Larutan Kenaikan Titik Didih
Soal No. 1
Natrium hidroksida 1,6 gram dilarutkan dalam 500 gram air. Hitung titik didih larutan tersebut! (Kb air = 0,520C/m, Ar Na = 23, Ar O = 16, Ar H = 1)
Pembahasan:
Diketahui:
gr = 1,6 gr
p = 500 gr
Kb = 0,520C/m
Ditanyakan: Tb ….?
Jawaban:
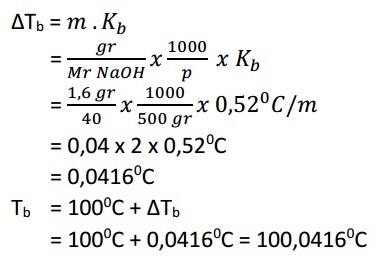
Soal No. 2
Sebanyak 1,41 gram zat organic dilarutkan dalam 20 gram aseton sehingga terjadi kenaikan titik didih 0,50C. Berapa Mr zat organic tersebut? (Kb Aseton = 1,670Ckg/mol)
Pembahasan:
Diketahui:
gr zat = 1,41 gr
gr aseton = 20 gr
Kb = 1,670C/m
∆Tb = 0,50C
Ditanyakan: Mr zat …?
Jawaban:

Soal No. 3
Untuk menaikkan titik didih 250 mL air menjadi 100,10C ditambahkan gula. Jika tekanan udara luar 1 atm (Kb = 0,50C/m), hitung jumlah zat gula yang harus ditambahkan!
Pembahasan:
Diketahui:
Tb = 100,10C
Kb = 0,50C/m
Mr gula = 342
P = 1 atm
V air = 250 mL
p = 1 gr/mL x 250 mL = 250 gr
Ditanyakan: gr gula…?
Jawaban:

Soal No. 4
Larutan urea 0,1 molal dalam air mendidih pada suhu 100,05 °C. Pada volume yang sama, larutan glukosa 0,1 molal dan sukrosa 0,3 molal dicampurkan. Hitung titik didih campuran tersebut!
Pembahasan:
Diketahui:
m urea = 0,1 molal
Tb = 100,050C
m glukosa = 0,1 molal
m sukrosa = 0,1 molal
Ditanyakan: Tb campuran …?
Jawaban:

Soal No. 5
Suatu zat X sebanyak 12,5 gram dilarutkan dalam 170 gram air sehingga titik didih larutan menjadi 100,630 Hitunglah Mr zat X tersebut! (Kb air = 0,5120C kg/mol)
Pembahasan:
Diketahui:
gr zat = 12,5 gr
gr air = 170 gr
Kb = 0,5120C.kg/mol
Tb = 100,630C
Ditanyakan: Mr zat …?
Jawaban:
