Soal UNBK Kimia 2018 dan Pembahasannya No. 1-5
Soal UN Kimia No. 1
Diketahui unsur 11X dan dapat berikatan dengan unsur 17Y, sifat fisik senyawa yang terbentuk dan jenis ikatannya berturut-turut adalah ….
A. lelehannya dapat menghantarkan listrik, ikatan ionik
B. larut dalam air, kovalen
C. tidak larut dalam air, ikatan ionik
D. larutannya menghantar listrik, kovalen
E. larutannya tidak menghantarkan listrik, ikatan ionik
Jawaban: A
Pembahasan:
Sebelum kita bahas soalnya, untuk kamu yang sedang mempersiapkan menghadapi ujian nasional. Kamu bisa mencoba latihan SOAL UN SMA 2020 terbaru yang telah disiapkan oleh Edutore.com. Selain itu, kamu juga dapat mencoba ribuan soal materi kimia secara gratis untuk mengasah pengetahuanmu mengenai kimia.
11X = 2 8 1 → X+
17Y = 2 8 7 → Y−
Itu artinya, senyawa X melepaskan 1 elektron dan senyawa Y menerima 1 elektron, jika mereka berikatan akan membentuk ikatan ionik.
X+ + Y− → XY
Adapun sifat ikatan ionik antara lain:
- larut dalam air
- menghantarkan listrik baik dalam bentuk lelehan maupun larutan
- titik didih dan titik leleh tinggi
Jadi, sifat fisik senyawa yang terbentuk dan jenis ikatannya berturut-turut adalah lelehannya dapat menghantarkan listrik, ikatan ionik (A).
Soal UN Kimia No. 2
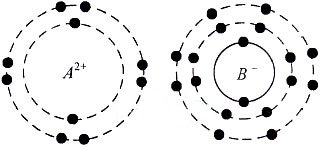
Dua ion yaitu A2+ dan B− memiliki lintasan elektron sebagai berikut:
Jika unsur A mempunyai jumlah neutron 12 dan B mempunyai jumlah neutron 18, pasangan data yang tepat adalah ….
| Unsur | Golongan | Periode | Notasi | |
| A. | A | IIA | 2 | 12A24 |
| B. | B | VIIIA | 3 | 18B36 |
| C. | A | IIA | 3 | 12A30 |
| D. | B | VIIA | 3 | 17B35 |
| E. | A | VIIIA | 2 | 18A36 |
Jawaban: D
Pembahasan:
Ion A2+ (melepas 2 elektron) mempunyai 10 elektron, maka:
- nomor atom : Z = 10 + 2 = 12
- nomor massa : A = 12 + 12 = 24
- notasi unsur : 12A24
- konfigurasi elektron : 1s2 2s2 2p6 3s2
- golongan : IIA
- periode : 3
Ion B− (menangkap 1 elektron) mempunyai 18 elektron, maka:
- nomor atom : Z = 18 − 1 = 17
- nomor massa : A = 17 + 18 = 35
- notasi unsur : 17B35
- konfigurasi elektron : 1s2 2s2 2p6 3s2 3p5
- golongan : VIIA
- periode : 3
Soal UN Kimia No. 3
Perhatikan konfigurasi elektron unsur X dan Y berikut!
X = 1s2 2s2 2p6 3s2 3p3
Y = 1s2 2s2 2p6 3s2 3p5
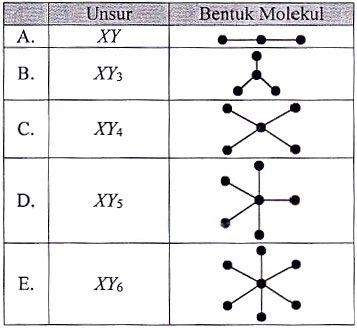
Jika kedua unsur tersebut bersenyawa, rumus kimia yang mungkin terjadi dan bentuk molekul senyawa yang benar adalah ….
Jawaban: D
Soal UN Kimia No. 4
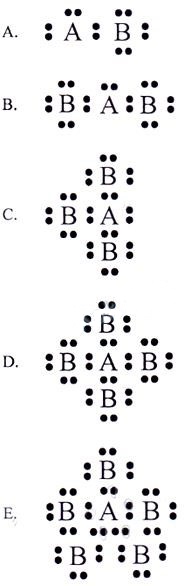
Jika unsur A (nomor atom 7) dan B (nomor atom 17) berikatan, struktur Lewis yang benar adalah ….
Jawaban: C
Pembahasan:
7A = 2, 5
17B = 2, 8, 7
Unsur A mempunyai 5 elektron valensi sehingga membutuhkan 3 elektron lagi agar terpenuhi kaidah oktet. Sedangkan unsur B mempunyai 7 elektron valensi sehingga membutuhkan 1 elektron lagi biar memenuhi kaidah oktet. Dengan demikian, senyawa yang terbentuk adalah AB3.
Struktur lewis AB3 ditunjukkan oleh opsi C.
Soal UN Kimia No. 5
Pada ruang tertutup dilakukan pembakaran 7 gram besi dengan 4 gram sulfur menghasilkan besi sulfida sebanyak 11 gram. Kenyataan ini sesuai dengan hukum dasar kimia, yaitu ….
A. Hukum Perbandingan Tetap (Proust)
B. Hukum Perbandingan Volume (Gay Lussac)
C. Hukum Kekekalan Massa (Lavoisier)
D. Hukum Perbandingan Berganda (Dalton)
E. Hukum Perbandingan Molekul (Avogadro)
Jawaban: C
Pembahasan:
Di soal dapat kita lihat bahwa massa zat sebelum dan sesudah reaksi memiliki jumlah yang sama. Sesuai dengan hukum kekekalan massa yang berbunyi:
“Massa zat-zat sebelum dan sesudah reaksi adalah sama”