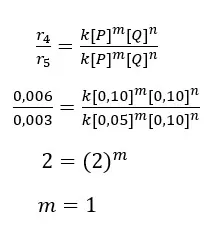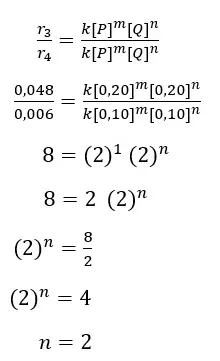Orde reaksi disebut juga tingkat reaksi yang menyatakan besarnya pengaruh konsentrasi dari zat yang bereaksi (reaktan) saat terjadi laju reaksi. Orde reaksi dapat berupa bilangan bulat positif kecil, namun dalam beberapa hal dapat berupa bilangan pecahan atau nol.
Nilai orde reaksi tidak dapat ditentukan dari harga koefisien reaksi, melainkan berdasarkan percobaan. Orde suatu reaksi merupakan penjumlahan dari orde reaksi setiap zat yang bereaksi. Orde reaksi bisa ditentukan dengan cara membandingkan data hasil percobaan laju reaksi terhadap konsentrasi reaktan.
Untuk mencari orde reaksi jika konsentrasi berbeda dapat kita lakukan dengan langkah-langkah sebagai berikut.
Misal, dalam suatu percobaan laju reaksi:
P + Q → Hasil
Diperoleh data sebagai berikut:
| No. | [P] (M) | [Q] (M) | Laju Reaksi (M/s) |
| 1 | 0,40 | 0,20 | 0,096 |
| 2 | 0,30 | 0,30 | 0,162 |
| 3 | 0,20 | 0,20 | 0,048 |
| 4 | 0,10 | 0,10 | 0,006 |
| 5 | 0,05 | 0,10 | 0,003 |
- Tentukanlah orde reaksinya
- Tentukanlah persamaan laju reaksinya
Pembahasan:
1. Orde Reaksi
Perhatikanlah bahwa konsentrasi P tidak ada yang sama, sedangkan konsentrasi Q ada yang sama, sehingga terlebih dahulu kita cari orde reaksi P. Kita cari dua data yang menunjukkan konsentrasi Q yang sama.
Sedangkan untuk mencari orde reaksi Q dipilih dua data P yang mana saja, tetapi bukan pada dua data Q yang sama, misal data no 3 dan 4.
Sehingga dihasilkan orde reaksi total = m + n = 1 + 2 = 3.
2. Persamaan Laju Reaksi
Untuk menuliskan persamaan laju reaksinya, kita tentukan terlebih dahulu tetapan laju reaksi dengan data percobaan 1.
r = k [P]m[Q]n
0,096 = k (0,40)1 (0,20)2
0,096 = k (0,40) (0,40)
0,096 = k 0,016
k = 0,096/0,016
k = 6
Setelah itu, dapat kita tuliskan persamaan laju reaksinya. Sehingga didapatkan persamaan laju reaksi sebagai berikut.
r = 6 [P][Q]2