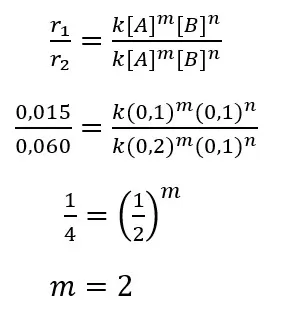Konstanta laju reaksi atau tetapan laju reaksi adalah tetapan yang harganya bergantung pada jenis pereaksi, suhu dan katalis. Tetapan laju reaksi berbanding terbalik dengan perubahan waktu. Semakin cepat reaksi berlangsung, maka harga tetapan laju reaksi semakin besar. Dan berbanding lurus dengan perubahan suhu. Semakin tinggi suhu reaksi, semakin besar harga tetapan laju reaksinya.
Cara menentukan tetapan laju reaksi dapat dilakukan setelah diketahui orde reaksi. Untuk lebih mudahnya perhatikan contoh soal berikut.
Suatu reaksi:
A + B → C
Data percobaan laju reaksinya:
| [A]awal (M) | [B]awal (M) | Laju Reaksi (M/detik) |
| 0,1 | 0,1 | 0,015 |
| 0,2 | 0,1 | 0,060 |
| 0,3 | 0,2 | 0,540 |
Tentukanlah:
- Orde reaksi A
- Harga tetapan laju reaksi
Pembahasan:
1. Orde reaksi A
4. Harga tetapan laju reaksi
r = k [A]2
0,015 = k (0,1)2
0,015 = k . 0,01
k = 0,015/0,01
k = 1,5