Katalis adalah zat yang dapat mempercepat laju reaksi. Katalis menurunkan energi aktivasi, sehingga jumlah tumbukan bertambah banyak dan reaksi dapat diselesaikan lebih cepat.
Katalis digolongkan sebagai katalis homogen dan heterogen. Katalis homogen adalah katalis yang memiliki fase yang sama dengan pereaksi dan bekerja melalui penggabungan dengan molekul atau ion pereaksi membentuk keadaan ‘antara’. Keadaan antara ini bergabung dengan pereaksi lainnya membentuk produk dan setelah produk dihasilkan, katalis melakukan regenerasi sebagai zat semula.
Suatu katalis heterogen adalah katalis yang berbeda fase dengan pereaksi dan produk. Katalis ini biasanya padatan dalam pereaksi gas atau cairan, dan reaksi terjadi pada permukaan katalis heterogen. Untuk alasan ini, katalis biasanya dipecah-pecah menjadi butiran halus.
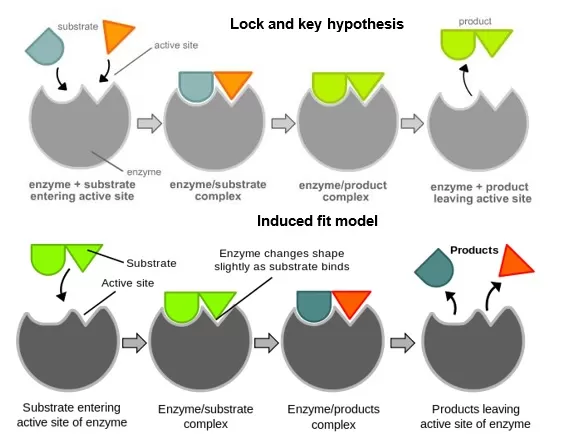
Dalam tubuh kita, berbagai proses kimia dipercepat oleh katalis yang disebut enzim (biokatalis). Enzim-enzim ini selalu bekerja secara spesifik; suatu reaksi hana dapat dipercepat oleh enzim tertentu, ibarat lubang kunci dengan anak kuncinya. Enzim membentuk kompleks dengan substrat (zat yang akan dipercepat reaksinya), lalu kompleks itu terurai menghasilkan zat yang diinginkan, sedangkan enzim dikembalikan lagi ke bentuknya semula. Contohnya:
- Enzim oksidase mempercepat reaksi oksidasi
- Enzim hidrolase mempercepat pemecahan bahan makanan melalui reaksi hidrolisis.
Dalam proses industri, penggunaan suhu yang lebih tinggi untuk mempercepat reaksi seperti proses Haber untuk sintesis ammonia bisa saja dilakukan, akan tetapi biaya operasionalnya akan menjadi sangat mahal.
Di dalam industri kimia, meningkatkan suhu berarti menambah biaya untuk pasokan energi. Oleh karena itu, diperlukan suatu zat yang mampu mempercepat reaksi tanpa harus meningkatkan suhu atau tekanan sehingga biaya produksi menjadi lebih murah.
Dalam proses kontak (reaksi pembuatan asam sulfat) ditambahkan katalis vanadium (V) oksida untuk mempercepat reaksi.
Dalam proses Haber-Bosch (pembuatan amonia) reaksi berjalan sangat lambat pada suhu rendah, sedangkan pada suhu tinggi gas NH3 yang dihasilkan cenderung terurai kembali menjadi gas nitrogen dan gas hidrogen. Sehingga ditambahkan katalis berupa serbuk besi (besi plus) yang menyebabkan produksi gas amonia dapat berlangsung efektif pada suhu 500°C.