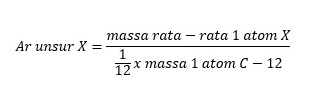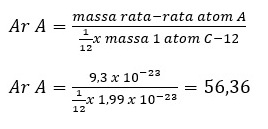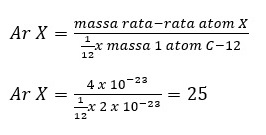Massa molar adalah perbandingan massa 1 molekul zat (unsur/senyawa) terhadap 1/12 x massa atom C-12 yang dinyatakan dalam gr/mol. Massa molar unsur dilambangkan dengan Ar (Massa Atom Relatif) dan massa molar senyawa dilambangkan dengan Mr (Massa Molekul Relatif). Massa molar dirumuskan sebagai berikut:
untuk massa atom relatif (Ar) adalah sebagai berikut:
Selain itu, massa atom relatif juga sudah tertera di tabel periodik unsur kimia, perhatikan potongan gambar tabel periodik berikut:
Sedangkan untuk massa molekul relatif (Mr) adalah sebagai berikut:
Mr = ∑Ar
Mari, perhatikan contoh soal menghitung massa molar berikut ini:
Soal No. 1
Massa rata-rata 1 atom unsur A adalah 9,3 x 10-23 gram dan massa 1 atom C-12 adalah 1,99 x 10-23 gram. Berapa massa molar unsur A tersebut?
Pembahasan:
Jadi, massa molar unsur A adalah 56,36.
Soal No. 2
Massa rata-rata 1 atom X adalah 4 x 10-23 gr, sedangkan massa 1 atom C-12 adalah 2 x 10-23 gr. Berapakah massa molar unsur X tersebut?
Pembahasan:
Jadi, massa molar unsur X adalah 25.
Soal No. 3
Berapa massa molekul relatif Ca(OH)2, Oksigen, H2SO4, CH3COOH, Al2(SO4)3, Al2, Na2CO3?
Pembahasan:
Mr Ca(OH)2 = (Ar Ca) + (2 x Ar O) + (2 x Ar H)
Mr Ca(OH)2 = (40) + (2 x 16) + (2 x 1) = 40 + 32 + 2 = 74
Mr Oksigen = 2 x Ar O = 2 x 16 = 32
Mr H2SO4 = (2 x Ar H) + (2 x Ar S) + (4 x Ar O)
Mr H2SO4 = (2 x 1) + ( 2 x 32) + (4 x 16) = 2 + 64 + 64 = 130
Mr CH3COOH = (2 x Ar C) + (4 x Ar H) + (2 x Ar O)
Mr CH3COOH = (2 x 12) + (4 x 1) + (2 x 16) = 24 + 4 + 32 = 60
Mr Al2(SO4)3 = (2 x Ar Al) + (3 x Ar S) + (12 x Ar O)
Mr Al2(SO4)3 = (2 x 27) + (3 x 32) + (12 x 16) = 54 + 96 + 192 = 342
Mr Al2 = 2 x Ar Al = 2 x 27 = 54
Mr Na2CO3 = (2 x Ar Na) + (1 x Ar C) + (3 x Ar O)
Mr Na2CO3 =(2 x 23) + (1 x 12) + (3 x 16) = 46 + 12 + 48 = 106
Soal No. 4
Berapa massa molekul relatif senyawa dengan rumus MgSO4.7H2O?
Pembahasan:
Mr MgSO4.7H2O = (1 x Ar Mg) + (1 x Ar S) + (4 x Ar O) + (14 x Ar H) + (7 x Ar O)
Mr MgSO4.7H2O = (1 x 24) + (1 x 32) + (4 x 16) + (14 x 1) + (7 x 16) = 24 + 32 + 64 + 14 + 112 = 246
Jadi, massa molekul relatif senyawa dengan rumus MgSO4.7H2O adalah 246.
Soal No. 5
Berapa massa molekul relatif untuk senyawa Ba3(PO4)2?
Pembahasan:
Mr Ba3(PO4)2 = (3 x Ar Ba) + (2 x Ar P) + (8 x Ar O)
Mr Ba3(PO4)2 = (3 x 137) + (2 x 31) + (8 x 16) = 411 + 62 + 128 = 601
Jadi, massa molekul relatif untuk senyawa Ba3(PO4)2 adalah 601