Berikut ini adalah 45 soal perubahan materi dan pemisahan campuran yang terdiri atas 30 soal pilihan ganda dan 15 soal essay yang telah dilengkapi dengan kunci jawabannya.
A. SOAL PILIHAN GANDA
Soal No. 1
Perubahan materi berikut yang termasuk perubahan kimia adalah ….
A. Garam dilarutkan dalam air
B. Bel listrik berdering
C. Lilin meleleh
D. Timah dipanaskan
E. Besi berkarat
Jawaban: E
Soal No. 2
Perhatikan perubahan materi berikut.
- Besi dibakar
- Kertas terbakar
- Air mendidih
- Kayu melapuk
- Kamper menguap
Perubahan yang termasuk perubahan fisika ditunjukkan oleh nomor ….
A. 1, 2, dan 5
B. 1, 3, dan 4
C. 1, 3, dan 5
D. 2, 3, dan 4
E. 3, 4, dan 5
Jawaban: C
Soal No. 3
Pernyataan berikut yang tidak tepat adalah ….
A. Semua materi memiliki massa
B. Semua materi memiliki energi
C. Massa tidak dipengaruhi gaya gravitasi
D. Pengertian massa dan berat sama
E. Perubahan kimia menyebabkan perubahan materi
Jawaban: D
Soal No. 4
Pernyataan berikut yang benar adalah ….
A. Unsur adalah zat tunggal
B. Campuran adalah zat tunggal
C. Larutan adalah campuran yang heterogen
D. Senyawa adalah campuran
E. Larutan dengan senyawa adalah sama
Jawaban: A
Soal No. 5
Tembaga digolongkan sebagai unsur karena ….
A. Homogen dan dapat diuraikan dengan reaksi kimia
B. Homogen dan tidak dapat diuraikan dengan reaksi kimia
C. Heterogen dan dapat diuraikan dengan reaksi kimia
D. Heterogen dan tidak dapat diuraikan dengan reaksi kimia
E. Heterogen dan dapat bereaksi dengan logam lain
Jawaban: B
Soal No. 6
Perbandingan berat besi dan belerang dalam besi (II) belerang adalah 7 : 4. Jika 5 gram besi direaksikan dengan 2 gram belerang, reaksi yang terjadi adalah ….
A. Terbentuk 7 gram besi belerang
B. Semua besi habis bereaksi
C. Semua besi dan belerang habis bereaksi
D. Terdapat sisa 1,5 gram besi
E. Terdapat sisa 1,5 gram belerang
Jawaban: D
Soal No. 7
Jumlah atom yang terdapat pada senyawa aluminium sulfat Al2(SO4)3 adalah ….
A. 9
B. 12
C. 14
D. 15
E. 17
Jawaban: E
Soal No. 8
Perbandingan unsur-unsur yang menyusun suatu senyawa selalu tetap merupakan bunyi dari hukum ….
A. Avogadro
B. Gay-lussac
C. Joseph Proust
D. John Dalton
E. Lavoisier
Jawaban: C
Soal No. 9
Campuran berikut yang dapat dipisahkan dengan cara kristalisasi adalah ….
A. Garam dapur dan air
B. Pasir dan air
C. Bensin dan parafin
D. Minyak dan susu
E. Tembaga dan besi
Jawaban: A
Soal No. 10
Peristiwa-peristiwa berikut yang mengalami perubahan kimia adalah ….
A. Garam dibakar
B. Besi dibakar
C. Pita magnesium dibakar
D. Timah dipanaskan
E. Lilin dipanaskan sampai meleleh
Jawaban: C
Soal No. 11
Sesuatu yang mempunyai massa dan menempati ruang adalah ….
A. Atom
B. Unsur
C. Molekul
D. Senyawa
E. Materi
Jawaban: E
Soal No. 12
Materi yang berupa zat tunggal yang tidak dapat diuraikan menjadi zat yang lebih sederhana dengan cara kimia biasa adalah ….
A. Unsur
B. Senyawa
C. Larutan
D. Koloid
E. Suspensi
Jawaban: A
Soal No. 13
Unsur yang memiliki sifat peralihan logam dan nonlogam disebut ….
A. Amfoter
B. Metaloid
C. Ion
D. Kation
E. Anion
Jawaban: B
Soal No. 14
Sifat berikut yang bukan merupakan sifat senyawa adalah ….
A. Heterogen
B. Merupakan zat tunggal
C. Terbentuk zat baru dari penyusunnya
D. Terbentuk dari dua unsur atau lebih dengan perbandingan tertentu
E. Komponennya dapat dipisah dengan cara kimia
Jawaban: A
Soal No. 15
Partikel-partikel penyusun materi adalah ….
A. Elektron dan proton
B. Elektron, proton, dan neutron
C. Atom dan molekul
D. Atom, molekul, dan ion
E. Ion positif dan ion negatif
Jawaban: B
Soal No. 16
Lambang atom yang sekarang digunakan merupakan hasil pemikiran ….
A. Dalton
B. Democritus
C. Aristoteles
D. Berzelius
E. Einstein
Jawaban: D
Soal No. 17
Pernyataan berikut yang merupakan ciri molekul unsur adalah ….
A. Terdiri atas satu jenis zat tunggal
B. Terdapat dua jenis zat tunggal
C. Disusun oleh dua jenis unsur
D. Terdiri atas satu jenis unsur
E. Terdiri atas lebih dua jenis unsur
Jawaban: D
Soal No. 18
Hal-hal berikut yang tidak membedakan atom logam dan atom nonlogam adalah ….
A. Daya hantar listriknya
B. Daya hantar panasnya
C. Wujud zat pada suhu kamar
D. Sifat kimianya
E. Kilapnya
Jawaban: E
Soal No. 19
Zat padat berikut yang bersifat rapuh adalah ….
A. Fosfor
B. Stronsium
C. Litium
D. Kromium
E. Argentum
Jawaban: A
Soal No. 20
Suatu logam pada suhu kamar berupa zat padat, berwarna kuning, dan dapat dipakai untuk membuah perhiasan. Lambang atom unsur tersebut adalah ….
A. Ag
B. Al
C. Ar
D. As
E. Au
Jawaban: E
Soal No. 21
Unsur-unsur berikut yang jika ditempa menjadi lempeng adalah ….
A. Ferrum
B. Neon
C. Argon
D. Fluorin
E. Fosforus
Jawaban: A
Soal No. 22
Unsur berikut yang memiliki sifat peralihan logam dan nonlogam adalah ….
A. Argentum
B. Xenon
C. Karbon
D. Berilium
E. Telurium
Jawaban: E
Soal No. 23
Materi berikut yang merupakan senyawa adalah ….
A. Air, alkohol, dan gula
B. Susu, santan, dan garam
C. Air, raksa, dan oksigen
D. Nitrogen, alkohol, dan gula
E. Santan, oksigen, dan timah
Jawaban: A
Soal No. 24
Materi berikut yang termasuk campuran homogen adalah ….
A. Udara
B. Air murni
C. Susu murni
D. Emas 24 karat
D. Cat air
Jawaban: A
Soal No. 25
Zat-zat berikut yang tidak termasuk unsur adalah ….
A. Alumunium
B. Neon
C. Xenon
D. Baja
E. Tembaga
Jawaban: D
Soal No. 26
Perhatikan perubahan materi dalam kehidupan sehari-hari berikut.
- Es mencair
- Gula dibakar
- Kamper menyublim
- Besi berkarat
- Proses pembuatan keju
Perubahan kimia ditunjukkan oleh nomor ….
A. 1, 2, dan 4
B. 1, 3, dan 5
C. 1, 4, dan 5
D. 2, 3, dan 4
E. 2, 4, dan 5
Jawaban: E
Soal No. 27
Perhatikan sifat-sifat materi berikut.
- Terbentuk dari dua macam zat atau lebih yang masih mempunyai sifat seperti zat asal.
- Dapat diuraikan menjadi zat yang lebih sederhana melalui reaksi kimia
- Terbentuk dari dua macam zat atau lebih dengan perbandingan massa tetap
- Terbentuk dari dua macam zat atau lebih dengan perbandingan massa yang berbeda
- Komponen-komponen penyusunnya dapat dipisahkan kembali secara fisika
Sifat senyawa ditunjukkan oleh nomor ….
A. 1 dan 2
B. 1 dan 3
C. 2 dan 3
D. 3 dan 4
E. 4 dan 5
Jawaban: C
Soal No. 28
Pemisahan campuran zat cair berdasarkan perbedaan titik didih disebut ….
A. Filtrasi
B. Distilasi
C. Kristalisasi
D. Kromatografi
E. Ekstraksi
Jawaban: B
Soal No. 29
Dalam 200 mg sampel batuan terkandung 10 mg perak dan 40 mg tembaga. Persentase emas dan tembaga dalam batuan itu adalah ….
A. 5% dan 20%
B. 5% dan 25%
C. 7,5% dan 25%
D. 7,5% dan 40%
E. 20% dan 40%
Jawaban: A
Soal No. 30
Jika 20 gram nikel dilarutkan dalam 180 gram pasir besi, persentase nikel yang terbentuk adalah ….
A. 8%
B. 10%
C. 11%
D. 12%
E. 18%
Jawaban: B
B. SOAL ESSAY
Soal No. 1
Materi adalah segala sesuatu yang mempunyai massa dan menempati ruang. Bagaimanakah cara membuktikan bahwa udara, air, dan gas LPG termasuk materi?
Jawaban:
Untuk membuktikan bahwa udara, air, dan gas LPG termasuk materi, kita dapat menggunakan beberapa eksperimen sederhana yang menunjukkan bahwa ketiganya memiliki massa dan menempati ruang.
1. Udara
- Memiliki Massa: Udara dapat dibuktikan memiliki massa dengan menimbang balon yang kosong, kemudian mengisi balon dengan udara (mengembungkannya), dan menimbangnya lagi. Jika dibandingkan, balon yang terisi udara akan memiliki berat yang lebih besar dibandingkan balon kosong, membuktikan bahwa udara memiliki massa.
- Menempati Ruang: Udara juga menempati ruang. Hal ini dapat dibuktikan dengan mengempiskan sebuah balon yang kemudian diisi udara. Saat udara masuk, balon akan mengembang karena udara membutuhkan ruang untuk menempati.
2. Air
- Memiliki Massa: Air jelas memiliki massa, yang dapat dibuktikan dengan menimbang wadah kosong, lalu menimbang wadah tersebut setelah diisi dengan air. Berat wadah akan bertambah setelah diisi air, menunjukkan bahwa air memiliki massa.
- Menempati Ruang: Air menempati ruang, yang dapat dilihat dengan jelas ketika kita menuangkan air ke dalam sebuah wadah. Air akan mengisi ruang di dalam wadah tersebut.
3. Gas LPG (Liquefied Petroleum Gas)
- Memiliki Massa: Untuk membuktikan bahwa gas LPG memiliki massa, kita bisa menimbang tabung LPG sebelum dan sesudah digunakan. Tabung yang penuh LPG akan lebih berat daripada tabung yang sudah sebagian digunakan, menunjukkan bahwa gas LPG memiliki massa.
- Menempati Ruang: Gas LPG juga menempati ruang. Hal ini terlihat dari fakta bahwa LPG disimpan dalam tabung yang khusus dirancang untuk menampungnya, dan jika tabung tersebut bocor, gas akan memenuhi ruang di sekitar tabung.
Ketiga contoh di atas menunjukkan bahwa udara, air, dan gas LPG memenuhi dua kriteria utama dari materi: mereka memiliki massa dan menempati ruang.
Soal No. 2
Apa perbedaan sifat fisis dan sifat kimia? Jelaskan berikut contohnya.
Jawaban:
Sifat fisis dapat diamati tanpa mengubah zat itu sendiri, sedangkan sifat kimia hanya dapat diamati ketika terjadi perubahan kimia pada zat tersebut. Sifat fisis berhubungan dengan keadaan fisik zat (seperti bentuk, ukuran, warna), sementara sifat kimia berhubungan dengan bagaimana zat tersebut bereaksi dengan zat lain atau berubah menjadi zat baru.
Soal No. 3
Jelaskan yang menyebabkan terjadinya perubahan wujud materi.
Jawaban:
Perubahan wujud materi terjadi karena adanya perubahan energi, khususnya energi panas (kalor). Perubahan ini dapat membuat zat berpindah dari satu fase ke fase lain, misalnya dari padat ke cair atau dari cair ke gas.
Soal No. 4
Jelaskan yang dimaksud dengan perubahan fisika dan berikan 5 contohnya
Jawaban:
Perubahan fisika adalah perubahan yang terjadi pada zat yang tidak mengubah identitas kimia atau komposisi kimia dari zat tersebut. Dalam perubahan fisika, zat mungkin mengalami perubahan bentuk, ukuran, fase, atau keadaan fisik lainnya, tetapi susunan molekul-molekul dalam zat tersebut tetap sama. Perubahan ini biasanya dapat dibalik (reversibel) dan tidak melibatkan reaksi kimia.
Contoh Perubahan Fisika
- Es Mencair: Ketika es (air dalam bentuk padat) dipanaskan, ia akan mencair menjadi air (bentuk cair). Meskipun terjadi perubahan dari padat ke cair, zat tersebut tetap merupakan air (H₂O).
- Air Menguap: Saat air dipanaskan hingga mencapai titik didihnya, ia berubah menjadi uap air (bentuk gas). Ini adalah perubahan dari cair ke gas, tetapi air tetap air secara kimia.
- Kayu di potong: Ketika kayu dipotong menjadi potongan-potongan yang lebih kecil, hanya ukuran dan bentuknya yang berubah. Komposisi kimia kayu tetap sama.
- Karet Meregang: Jika sepotong karet direntangkan, panjang dan bentuk karet akan berubah. Namun, setelah dilepaskan, karet bisa kembali ke bentuk semula, dan komposisi kimianya tetap tidak berubah.
- Air membeku: Air yang didinginkan di bawah titik beku akan berubah menjadi es. Ini adalah perubahan dari cair ke padat, tetapi air tetaplah air secara kimiawi.
Soal No. 5
Jelaskan yang dimaksud dengan perubahan kimia dan berikan 5 contohnya
Jawaban:
Perubahan kimia adalah perubahan yang terjadi ketika satu atau lebih zat mengalami transformasi menjadi zat baru dengan komposisi kimia yang berbeda. Dalam perubahan kimia, terjadi reaksi kimia yang menghasilkan produk dengan sifat-sifat yang berbeda dari zat asalnya. Perubahan ini biasanya tidak dapat dibalik (irreversible) melalui cara fisik sederhana, karena zat-zat baru yang terbentuk memiliki struktur molekul yang berbeda dari zat asalnya.
Contoh Perubahan Kimia
- Kertas di bakar: Ketika kertas dibakar, ia berubah menjadi abu, gas karbon dioksida, dan uap air. Proses ini melibatkan reaksi dengan oksigen dan menghasilkan zat-zat baru yang tidak dapat kembali menjadi kertas.
- Besi berkarat: Ketika besi terpapar udara dan kelembaban dalam jangka waktu lama, ia bereaksi dengan oksigen dan air untuk membentuk karat (besi oksida). Karat ini adalah zat baru yang berbeda dari besi asli.
- Pembuatan Roti: Selama proses pemanggangan, bahan-bahan seperti tepung, gula, dan ragi mengalami reaksi kimia, termasuk fermentasi oleh ragi yang menghasilkan gas karbon dioksida, sehingga roti mengembang. Setelah dipanggang, roti tidak bisa diubah kembali menjadi bahan asalnya.
- Fotosintesis pada Tumbuhan: Dalam proses fotosintesis, tumbuhan menggunakan sinar matahari, karbon dioksida, dan air untuk membentuk glukosa dan oksigen. Proses ini menghasilkan zat baru, yaitu glukosa, yang berbeda secara kimia dari bahan-bahan awalnya.
- Reaksi Asam dan Basa: Ketika asam (misalnya, asam klorida) bereaksi dengan basa (misalnya, natrium hidroksida), mereka membentuk air dan garam (natrium klorida). Produk yang terbentuk (air dan garam) berbeda dari zat-zat awalnya.
Soal No. 6
Tuliskan masing-masing 5 perubahan kimia yang menguntungkan dan yang merugikan
Jawaban:
Berikut adalah contoh-contoh perubahan kimia yang menguntungkan dan yang merugikan:
Perubahan Kimia yang Menguntungkan
- Fotosintesis: Proses fotosintesis pada tumbuhan mengubah karbon dioksida dan air menjadi glukosa dan oksigen, yang sangat penting untuk kehidupan di Bumi. Glukosa digunakan sebagai sumber energi, dan oksigen yang dilepaskan diperlukan oleh makhluk hidup untuk bernapas.
- Pembuatan Pupuk: Proses kimia seperti sintesis amonia melalui proses Haber-Bosch memungkinkan produksi pupuk nitrogen dalam jumlah besar, yang meningkatkan hasil pertanian dan membantu memenuhi kebutuhan pangan dunia.
- Fermentasi: Proses fermentasi mengubah gula menjadi alkohol dan karbon dioksida. Ini digunakan dalam pembuatan produk seperti roti, bir, anggur, dan yogurt, yang sangat bernilai dalam industri pangan.
- Produksi Obat-obatan: Reaksi kimia digunakan untuk sintesis obat-obatan penting yang menyelamatkan nyawa dan meningkatkan kesehatan manusia. Contohnya adalah pembuatan antibiotik seperti penicillin yang membantu melawan infeksi bakteri.
- Proses Pengolahan Logam: Ekstraksi logam seperti besi dan aluminium dari bijihnya melalui proses kimia memungkinkan pembuatan bahan konstruksi, kendaraan, dan berbagai alat yang sangat penting untuk pembangunan infrastruktur dan industri.
Perubahan Kimia yang Merugikan
- Perkaratan Besi: Besi yang bereaksi dengan oksigen dan air menghasilkan karat (besi oksida), yang menyebabkan kerusakan pada struktur bangunan, kendaraan, dan peralatan, mengurangi kekuatan dan usia pakai material tersebut.
- Pembusukan Makanan: Makanan yang terurai melalui reaksi kimia oleh mikroorganisme menyebabkan pembusukan, yang tidak hanya merusak makanan tetapi juga dapat menimbulkan risiko kesehatan jika dikonsumsi.
- Pencemaran Udara: Pembakaran bahan bakar fosil seperti batubara dan minyak bumi menghasilkan zat berbahaya seperti karbon dioksida, nitrogen oksida, dan sulfur dioksida, yang berkontribusi pada polusi udara, hujan asam, dan perubahan iklim.
- Keracunan Pestisida: Penggunaan pestisida yang berlebihan atau tidak tepat menyebabkan akumulasi bahan kimia beracun di lingkungan, yang dapat merusak ekosistem, mencemari air, dan berbahaya bagi kesehatan manusia dan hewan.
- Oksidasi Lemak (Rancidity): Lemak dan minyak dalam makanan dapat mengalami oksidasi, menghasilkan zat yang berbau dan berasa tidak enak, serta dapat menghasilkan senyawa berbahaya bagi kesehatan jika dikonsumsi.
Perubahan kimia memiliki dampak yang sangat luas, baik yang bermanfaat maupun yang merugikan. Mengelola perubahan kimia yang merugikan dan memanfaatkan yang menguntungkan adalah tantangan penting dalam banyak bidang, termasuk lingkungan, industri, dan kesehatan.
Soal No. 7
Perubahan materi selalu diiringi oleh perubahan energi. Jelaskan maksudnya.
Jawaban:
Pernyataan bahwa “perubahan materi selalu diiringi oleh perubahan energi” mengacu pada prinsip dasar dalam ilmu fisika dan kimia yang menyatakan bahwa setiap kali materi mengalami perubahan, baik itu perubahan fisika maupun kimia, selalu ada perubahan dalam bentuk atau jumlah energi yang terlibat.
Soal No. 8
Jelaskan perbedaan unsur dengan senyawa. Berikan masing-masing 10 contoh unsur dan senyawa berikut rumus kimianya.
Jawaban:
Unsur dan senyawa adalah dua jenis zat murni yang menjadi dasar dari semua materi di alam semesta. Berikut penjelasan perbedaannya serta contoh-contohnya:
Unsur adalah zat murni yang terdiri dari atom-atom sejenis. Setiap unsur memiliki jumlah proton yang sama dalam inti atomnya, yang disebut nomor atom. Unsur tidak dapat diuraikan menjadi zat yang lebih sederhana melalui reaksi kimia biasa. Contoh Unsur:
- Hidrogen (H): Unsur paling ringan dan paling melimpah di alam semesta.
- Oksigen (O): Unsur yang sangat penting untuk respirasi makhluk hidup.
- Karbon (C): Unsur dasar dalam semua senyawa organik.
- Nitrogen (N): Unsur yang membentuk sekitar 78% dari atmosfer Bumi.
- Helium (He): Gas mulia yang ringan, digunakan dalam balon udara.
- Besi (Fe): Unsur logam yang digunakan dalam pembuatan baja.
- Emas (Au): Logam mulia yang sangat berharga dan tidak mudah bereaksi.
- Klorin (Cl): Unsur yang berperan dalam disinfeksi air dan pembuatan garam.
- Aluminium (Al): Unsur logam ringan yang banyak digunakan dalam industri.
- Kalsium (Ca): Unsur yang penting dalam pembentukan tulang dan gigi.
Senyawa adalah zat murni yang terbentuk dari dua atau lebih unsur yang bergabung secara kimia dengan perbandingan tertentu. Senyawa dapat diuraikan menjadi unsur-unsurnya melalui reaksi kimia. Contoh Senyawa:
- Air (H₂O): Senyawa yang sangat penting bagi kehidupan, terdiri dari hidrogen dan oksigen.
- Karbon dioksida (CO₂): Gas yang terbentuk dari karbon dan oksigen, dihasilkan dalam respirasi dan pembakaran.
- Garam dapur (NaCl): Senyawa yang terdiri dari natrium dan klorin, digunakan sebagai bumbu makanan.
- Asam klorida (HCl): Senyawa yang terdapat dalam lambung dan digunakan dalam berbagai proses industri.
- Amonia (NH₃): Senyawa yang terdiri dari nitrogen dan hidrogen, digunakan dalam pembuatan pupuk.
- Metana (CH₄): Gas yang merupakan senyawa karbon dan hidrogen, dikenal sebagai komponen utama gas alam.
- Glukosa (C₆H₁₂O₆): Senyawa gula sederhana yang berperan sebagai sumber energi utama bagi sel.
- Kalsium karbonat (CaCO₃): Senyawa yang terdapat dalam batu kapur dan digunakan dalam pembuatan semen.
- Asam sulfat (H₂SO₄): Senyawa yang sangat penting dalam industri, digunakan dalam pembuatan pupuk, bahan kimia, dan dalam baterai.
- Etil alkohol (C₂H₅OH): Senyawa yang digunakan dalam minuman beralkohol, antiseptik, dan bahan bakar.
Soal No. 9
Bagaimana cara membedakan senyawa dengan campuran? Berikan contohnya, ciri khas apa yang dimiliki senyawa?
Jawaban:
Untuk membedakan senyawa dari campuran, perhatikan apakah zat tersebut memiliki perbandingan unsur yang tetap dan apakah zat-zat penyusunnya dapat dipisahkan dengan cara fisik atau tidak. Jika zat tersebut memiliki perbandingan yang tetap dan tidak dapat dipisahkan dengan metode fisik, maka itu adalah senyawa. Sebaliknya, jika zat tersebut bisa dipisahkan secara fisik dan tidak memiliki perbandingan tetap, itu adalah campuran.
Contoh senyawa: Karbon dioksida (CO₂), glukosa (C₆H₁₂O₆), dan metana (CH₄).
Contoh campuran: Campuran pasir dan air, minyak dan air, serta salad buah.
Ciri khas senyawa:
- Kepemilikan sifat unik: Senyawa memiliki sifat-sifat unik yang tidak dimiliki oleh unsur-unsurnya secara individu. Misalnya, air (H₂O) sebagai senyawa memiliki titik didih yang berbeda dari hidrogen dan oksigen.
- Stabilitas kimia: Senyawa biasanya lebih stabil secara kimia dibandingkan dengan unsur-unsurnya dalam keadaan bebas.
- Metode pemisahan: Senyawa hanya dapat diuraikan menjadi unsur-unsurnya melalui reaksi kimia, seperti elektrolisis pada air untuk menghasilkan hidrogen dan oksigen. Sebaliknya, campuran dapat dipisahkan melalui metode fisik seperti filtrasi, distilasi, atau kromatografi.
Soal No. 10
Apa sarat terbentuknya larutan? Adakah larutan yang tidak berwujud cair? Berikan 5 contohnya.
Jawaban:
Syarat terbentuknya larutan:
- Pelarut dan Zat Terlarut: Larutan terbentuk dari campuran dua atau lebih zat, di mana satu zat (zat terlarut) larut dalam zat lain (pelarut).
- Kesetimbangan Fasa: Zat terlarut harus dapat tersebar secara merata dalam pelarut, sehingga tidak ada batas fasa yang jelas antara zat terlarut dan pelarut.
- Interaksi Molekul: Ada interaksi yang cukup kuat antara molekul zat terlarut dan pelarut, sehingga molekul zat terlarut dapat menyebar secara merata dalam pelarut.
- Energi Pembentukan Larutan: Energi yang dilepaskan saat pembentukan larutan harus lebih besar atau setidaknya seimbang dengan energi yang dibutuhkan untuk memutus ikatan antara molekul zat terlarut dan molekul pelarut.
Contoh larutan yang tidak berwujud cair:
- Larutan Gas dalam Gas: Udara atmosfer adalah contoh larutan di mana oksigen, nitrogen, dan gas-gas lain larut dalam nitrogen (sebagai pelarut utama).
- Larutan Gas dalam Padatan: Hidrogen yang diserap oleh logam paladium. Hidrogen larut dalam struktur kristal logam.
- Larutan Padat dalam Padat (Paduan): Kuningan adalah paduan (larutan padat) yang terdiri dari tembaga dan seng.
- Larutan Padat dalam Gas: Kabut dan aerosol adalah larutan padatan kecil yang tersebar dalam gas.
- Larutan Gas dalam Padatan (Gelembung di Kaca): Gelembung gas yang terperangkap dalam kaca selama proses pembuatannya.
Dengan contoh-contoh ini, bisa dilihat bahwa larutan tidak selalu harus berbentuk cair.
Soal No. 11
Tuliskan bagaimana caranya melakukan pemisahan campuran.
Jawaban:
Pemisahan campuran adalah proses untuk memisahkan komponen-komponen dalam campuran berdasarkan sifat fisik mereka. Ada beberapa metode pemisahan campuran yang umum digunakan, yaitu:
- Filtrasi. Prinsip kerja filtrasi adalah memisahkan zat padat yang tidak larut dari cairan atau gas dengan menggunakan saringan (filter). Contohnya memisahkan pasir dari air dengan menggunakan kertas saring.
- Distilasi. Prinsip kera distilasi adalah memisahkan komponen berdasarkan perbedaan titik didihnya. Campuran dipanaskan hingga salah satu komponen menguap, kemudian uapnya didinginkan kembali menjadi cairan (kondensasi). Contohnya memisahkan air dari garam melalui distilasi air laut.
- Kromatografi. Prinsip kerja kromatofrafi adalah memisahkan komponen campuran berdasarkan perbedaan laju pergerakan masing-masing komponen saat melewati media stasioner dengan bantuan fase gerak. Contohnya memisahkan pewarna dalam tinta dengan menggunakan kromatografi kertas.
- Sentrifugasi. Prinsip kerja sentrifugasi adalah memisahkan zat berdasarkan perbedaan kepadatannya dengan cara memutar campuran pada kecepatan tinggi. Contohnya memisahkan darah menjadi plasma dan sel darah merah.
- Ekstraksi. Prinsip kerja ekstrasi adalah memisahkan zat berdasarkan perbedaan kelarutan dalam dua pelarut yang tidak saling bercampur. Contohna memisahkan minyak esensial dari daun dengan menggunakan pelarut organik.
- Sublimasi. Prinsip kerja sublimasi adalah memisahkan zat yang dapat menyublim dari zat lainnya dengan cara memanaskan campuran sehingga zat yang menyublim menguap dan kemudian dikondensasikan kembali. Contohnya memisahkan yodium dari campurannya dengan pasir.
Setiap metode ini digunakan tergantung pada jenis dan sifat dari komponen-komponen yang ada dalam campuran.
Soal No. 12
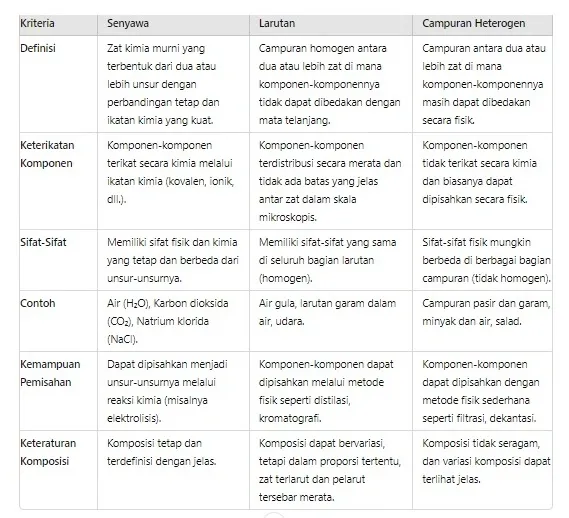
Tuliskan persamaan dan perbedaan senyawa, larutan, dan campuran heterogen
Jawaban:
Persamaan senyawa, larutan, dan campuran heterogen
- Terbentuk dari Dua atau Lebih Zat: Baik senyawa, larutan, maupun campuran heterogen semuanya terbentuk dari kombinasi dua atau lebih zat.
- Mengandung Berbagai Komponen: Ketiganya memiliki lebih dari satu jenis komponen, meskipun dalam proporsi dan pengaturan yang berbeda.
- Dapat Dipisahkan dengan Cara Tertentu: Dalam kasus tertentu, senyawa, larutan, dan campuran heterogen dapat dipisahkan menjadi komponen-komponennya dengan metode yang tepat (misalnya, pemisahan kimia untuk senyawa, pemisahan fisik untuk larutan dan campuran heterogen).
Persamaan senyawa, larutan, dan campuran heterogen
Soal No. 13
Bagaimana caranya memisahkan zat warna?
Jawaban:
Memisahkan zat warna biasanya dilakukan menggunakan metode kromatografi, karena metode ini efektif untuk memisahkan komponen-komponen berdasarkan perbedaan sifat fisiknya, seperti kelarutan dan interaksi dengan fase stasioner.
Soal No. 14
Jelaskan perbedaan analisis kualitatif dan analisis kuantitatif. Tuliskan contohnya.
Jawaban:
Perbedaan Analisis Kualitatif dan Analisis Kuantitatif:
- Analisis kualitatif mengidentifikasi apa yang ada. Sedangkan analisis kuantitatif mengukur berapa banyak yang ada.
- Analisis kualitatif hasilnya berupa deskripsi (jenis zat, identitas komponen). Sedangkan analisis kuantitatif hasilnya berupa angka (konsentrasi, massa, volume).
- Analisis kualitatif lebih fokus pada pengamatan dan pengenalan karakteristik zat. Sedangkan analisis kuantitatif lebih fokus pada pengukuran dan analisis data numerik.
Contoh Kasus:
- Analisis Kualitatif: Seorang ahli kimia ingin mengetahui apakah suatu sampel air mengandung ion klorida. Dia melakukan uji dengan menambahkan larutan perak nitrat (AgNO₃). Jika ion klorida ada, akan terbentuk endapan putih perak klorida (AgCl).
- Analisis Kuantitatif: Setelah mengetahui bahwa ada ion klorida dalam air, ahli kimia tersebut kemudian melakukan titrasi argentometri untuk menentukan berapa banyak ion klorida yang ada dalam sampel air tersebut, misalnya dalam mg/L.
Soal No. 15
Suatu soda kue sebanyak 200 gram diuji dengan analisis volumetri untuk mengetahui kadar NaHCO3 dalam soda kue. Jika dari hasil analisis diketahui massa NaHCO3 sebesar 160 gram tentukan kadarnya.
Jawaban: