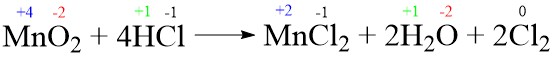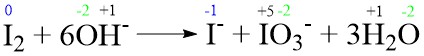Untuk lebih meningkatkan pemahamanmu mengenai materi reaksi redoks, pelajarilah soal redoks pilihan ganda dan pembahasannya berikut ini.
Soal No. 1
Di antara reaksi-reaksi di bawah ini yang merupakan reaksi redoks adalah ….
A. CuO + 2HCl → CuCl2 + H2O
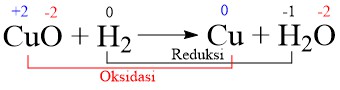
B. CuO + H2 → Cu + H2O
C. NaOH + Ag+ → AgOH + Na+
D. Fe2O3 + 3H2SO4 → Fe2(SO4)3 + H2O
E. ZnO + 2HCl → ZnCl2 + H2O
Jawaban: B
Pembahasan:
Soal No. 2
Bilangan oksidasi atom S yang paling tinggi terdapat pada ….
A. SO2
B. S2O32-
C. S4O62-
D. SO42-
E. H2S
Jawaban: D
Pembahasan:
A. SO2
SO2 = biloks S + 2 biloks O
0 = S + (2 x (-2)
0 = S – 4
S = +4
B. S2O32-
S2O32- = 2biloks S + 3biloks O
-2 = (2 x S) + (3 x (-2))
-2 = 2S – 6
2S = +4
S = 4/2 = +2
C. S4O62-
S4O62- = 4biloks S + 6biloks O
-2 = (4 x S) + (6 x (-2))
-2 = 4S – 12
4S = +10
S = 10/4 = +2,5
D. SO42-
SO42- = biloks S + 4biloks O
-2 = S + (4 x (-2))
-2 = S – 8
S = 8 – 2 = +6
E. H2S
H2S = 2biloks H + biloks S
0 = (2 x 1) + S
0 = 2 + S
S = -2
Soal No. 3
Bilangan oksidasi I di dalam ion IO3– adalah ….
A. +5
B. +3
C. +1
D. -1
E. -5
Jawaban: A
Pembahasan:
IO3– = biloks I + 3biloks O
-1 = I + (3 x (-2))
-1 = I – 6
I = 6 -1 = +5
Soal No. 4
Bilangan oksidasi atom Cr yang sama dengan bilangan oksidasi atom Mn yang terdapat pada senyawa MnO42- adalah ….
A. CrO
B. CrCl3
C. Cr2O72–
D. Cr2(SO4)3
E. Cr(NO3)2
Jawaban: C
Pembahasan:
Kita cari dulu biloks Mn.
MnO42- = biloks Mn + 4biloks O
-2 = Mn + (4 x (-2))
-2 = Mn – 8
Mn = 8 – 2 = +6
Jadi biloks Mn adalah +6. Maka kita cari biloks Cr yang nilainya +6 juga.
A. CrO
CrO = biloks Cr + biloks O
0 = Cr + (-2)
0 = Cr – 2
Cr = +2
B. CrCl3
CrCl3 = biloks Cr + 3biloks Cl
0 = Cr + (3 x (-1))
0 = Cr – 3
Cr = +3
C. Cr2O72–
Cr2O72– = 2biloks Cr + 7biloks O
-2 = (2 x Cr) + (7 x (-2))
-2 = 2Cr – 14
2Cr = 14 – 2
Cr = 12/2 = +6
D. Cr2(SO4)3
Cr2(SO4)3 = 2biloks Cr + 3biloks SO42–
0 = 2Cr + (3 x (-2)
0 = 2Cr – 6
Cr = 6/2 = +3
E. Cr(NO3)2
Cr(NO3)2 = biloks Cr + 2biloks NO3–
0 = Cr + (2 x (-1))
0 = Cr – 2
Cr = +2
Soal No. 5
Bilangan oksidasi tertinggi atom mangan terdapat pada ….
A. MnO
B. MnO2
C. MnSO4
D. KMnO4
E. K2MnO4
Jawaban: D
Pembahasan:
A. MnO
MnO = biloks Mn + biloks O
0 = Mn + (-2)
Mn = +2
B. MnO2
MnO2 = biloks Mn + 2biloks O
0 = Mn + 2 (-2)
0 = Mn – 4
Mn = +4
C. MnSO4
MnSO4 = biloks Mn + biloks S + 4biloks O
0 = Mn + 6 + (4 x (-2))
0 = Mn + 6 – 8
Mn = +2
D. KMnO4
KMnO4 = biloks K + biloks Mn + 4biloks O
0 = 1 + Mn + (4 x (-2))
0 = 1 + Mn – 8
Mn = +7
E. K2MnO4
K2MnO4 = 2biloks K + biloks Mn + 4biloks O
0 = (2 x 1) + Mn + (4 x (-2))
0 = 2 + Mn – 8
Mn = +6
Soal No. 6
Pada reaksi redoks:
MnO2 + 4HCl → MnCl + 2H2O + 2Cl2
Bilangan oksidasi Mn mengalami perubahan dari ….
A. +4 menjadi +2
B. +4 menjadi +1
C. +2 menjadi +4
D. +2 menjadi +1
E. +2 menjadi +4
Jawaban: A
Pembahasan:
Soal No. 7
Nama dari senyawa SnO2 yang paling tepat adalah ….
A. Seng (IV) oksida
B. Seng (II) oksida
C. Timah (IV) oksida
D. Timah (II) oksida
E. Timbal (IV) oksida
Jawaban: C
Pembahasan:
Sn adalah timah dengan bilangan oksidasi +4 maka diberi nama Timah (IV). Sedangkan O adalah oksigen maka diberi nama oksigen dengan akhiran -ida sehingga menajdi oksida. Jadi nama yang tepat untuk SnO2 adalah Timah (IV) oksida.
Soal No. 8
Di antara senyawa berikut yang atom hidrogennya mempunyai bilangan oksidasi -1 adalah ….
A. H2O
B. Fe(OH)3
C. AlH3
D. H2S
E. Mg(OH)2
Jawaban: C
Pembahasan:
A. H2O
H2O = 2biloks H + biloks O
0 = 2H + (-2)
0 = 2H – 2
H = 2/2 = +1
B. Fe(OH)3
Fe(OH)3 = biloks Fe + 3biloks O + 3biloks H
0 = 3 + (3 x (-2) + 3H
0 = 3 – 6 + 3H
H = 3/3 = +1
C. AlH3
AlH3 = biloks Al + 3biloks H
0 = 3 + 3H
3H = -3
H = -3/3 = -1
D. H2S
H2S = 2biloks H + biloks S
0 = 2H – 2
H = 2/2 = +1
E. Mg(OH)2
Mg(OH)2 = biloks Mg + 2bilok O + 2biloks H
0 = 2 + (2 x (-2)) + 2H
0 = 2 – 4 + 2H
2H = 2
H = 2/2 = +1
Soal No. 9
Rumus kimia dari besi (III) sulfat adalah ….
A BiSO4
B. Bi2(SO4)3
C. FeSO4
D. Fe3(SO4)2
E. Fe2(SO4)3
Jawaban: E
Pembahasan:
Besi (III) = Fe3+
sulfat = SO42-
Jadi, besi (III) sulfat adalah Fe2(SO4)3.
Soal No. 10
Dalam reaksi:
I2 + 6OH– → I– + IO3– + 3H2O
bilangan oksidasi I berubah dari …
A. 0 menjadi +5 dan -1
B. 0 menjadi +4 dan -1
C. 0 menjadi +3 dan -1
D. +1 menjadi -5 dan -1
E. -1 menjadi +5 dan +1
Jawaban: A
Pembahasan: