Cara menentukan nomor atom dan nomor massa. Suatu atom terdiri dari sebuah inti yang sangat padat yang tersusun atas proton dan neutron, ditambah elektron yang bergerak di sekitar inti pada jarak yang relatif jauh dari inti. Proton bermuatan positif, neutron tidak bermuatan, dan elektron bermuatan negatif. Proton dan neutron memiliki massa yang kira – kira sama, yaitu sekitar 1840 kali lebih besar dari massa elektron.
1. Nomor Atom (Z)
Nomor atom (Z) suatu unsur adalah jumlah proton dalam inti atom dari unsur tersebut. Nomor atom menentukan identitas suatu unsur, karena atom bersifat netral maka jumlah proton sama dengan jumlah elektronnya.
Sehingga nomor atom juga menunjukkan jumlah elektron. Elektron inilah yang nantinya paling menentukan sifat suatu unsur. Contohnya, atom oksigen mempunyai 8 proton dan 8 elektron, sehingga nomor atomnya 8.
Secara matematika, cara menentukan nomor atom dapat dirumuskan sebagai berikut:
Nomor Atom (Z) = Nomor Massa – Jumlah Neutron
2. Nomor Massa (A)
Nomor massa adalah hasil penjumlahan antara jumlah proton dan jumlah neutron dalam inti. Contohnya, atom oksigen mempunyai nomor atom 8 dan nomor massa 16, sehingga atom oksigen mengandung 8 proton dan 8 neutron.
Secara matematika, cara menentukan nomor massa (A) dapat dirumuskan sebagai berikut:
Nomor Massa (A) = Nomor Atom + Jumlah Neutron
Penulisan lambang atom unsur menyertakan nomor atom dan nomor massa.
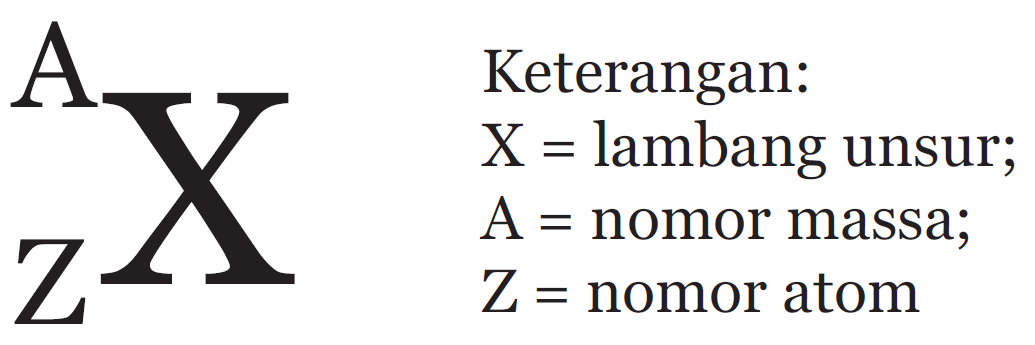
Untuk lebih memahami materi nomor atom dan nomor massa, perhatikan contoh soal nomor atom dan nomor massa berikut ini:
Contoh Soal
Hitunglah jumlah proton, elektron, dan neutron dari unsur – unsur berikut!
- 3919K
- 2713Al
- 5626Fe
Pembahasan:
1. 3919K
Jumlah proton = 19
Jumlah elektron = 19
Jumlah neutron = 39 – 19 = 20
2. 5626Al
Jumlah proton = 13
Jumlah elektron = 13
Jumlah neutron = 27 – 13 = 14
3. 5626Fe
Jumlah proton = 26
Jumlah elektron = 26
Jumlah neutron = 56 – 26 = 30