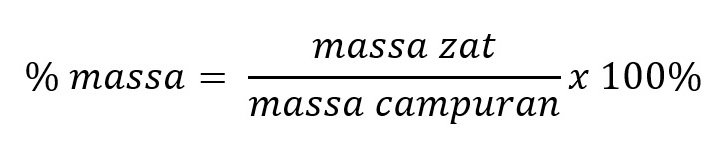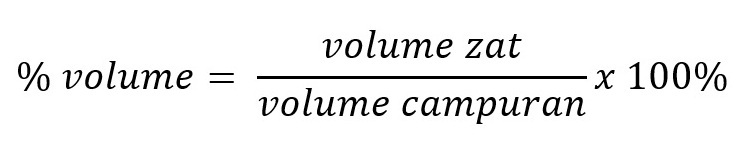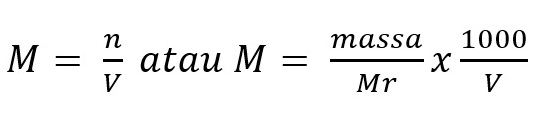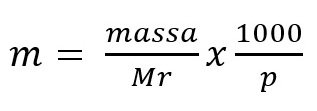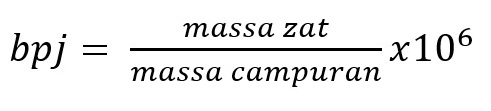Jenis satuan konsentrasi dibagi menjadi 6, yaitu: persen massa (%), persen volume (%), molaritas (M), molalitas (m), bagian per sejuta (bpj), dan fraksi mol (X).
1. Persen Massa (%)
Satuan persen massa merupakan perbandingan dari dua kuantitas yang sama dan dapat dirumuskan sebagai berikut:
2. Persen Volume (%)
Satuan persen volume digunakan untuk menyatakan konsentrasi zat yang terbentuk dari dua wujud zat cair. Persen volume dirumuskan sebagai berikut.
3. Molaritas (M)
Satuan molaritas didefinisikan sebagai banyaknya mol zat terlarut dalam 1 L larutan; artinya molaritas dirumuskan sebagai berikut.
Keterangan:
M = Molaritas (M)
n = jumlah mol (mol)
V = volume zat (L)
4. Molalitas (m)
Molalitas dapat didefinisikan sebagai banyaknya mol zat terlarut yang dilarutkan dalam 1 kg (1000 g) pelarut.
Keterangan:
m = molalitas (m)
massa = massa zat (gram)
Mr = massa molekul relatif
p = massa pelarut (gram)
Misalnya, untuk menyiapkan 1 molal, atau 1 m larutan berair natrium sulfat (Na2SO4), kita perlu melarutkan 1 mol (142 g) zat tersebut dalam 1000 g air. Bergantung pada jenis interaksi zat terlarut-pelarut, volume akhir larutan bisa lebih atau kurang dari 1000 mL. Juga dimungkinkan, meskipun jarang terjadi, bahwa volume akhir sama dengan 1000 mL.
5. Bagian per Sejuta (bpj) atau Part per Million (ppm)
Bagian per sejuta atau part per million merupakan perbandingan satu bagian zat komponen dengan satu bagian campuran. Bagian per sejuta di rumuskan sebagai berikut.
6. Fraksi Mol (X)
Fraksi mol menyatakan perbandingan jumlah mol zat terlarut dan mol zat pelarut terhadap jumlah mol larutan. Fraksi mol (X) dirumuskan sebagai berikut.