Energi ionisasi dan afinitas elektron adalah dua konsep yang terkait dengan sifat-sifat atom dan molekul dalam kimia.
1. Energi Ionisasi
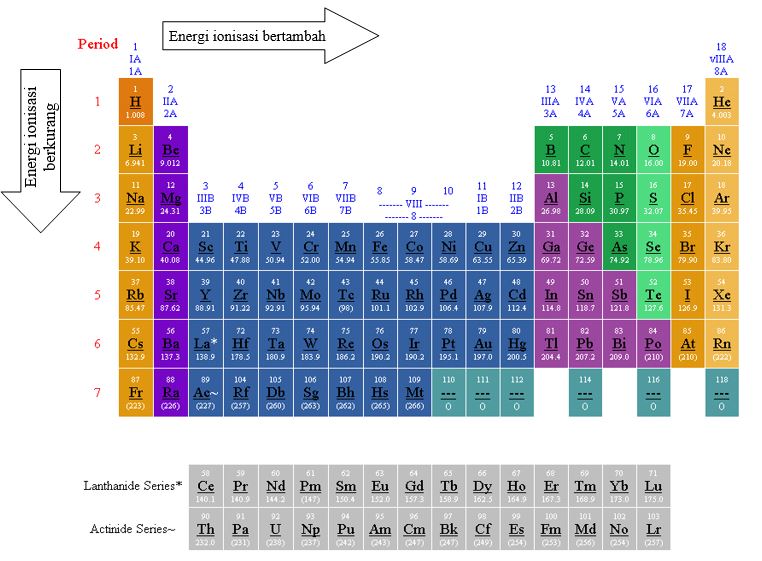
Pengertian energi ionisasi adalah energi yang diperlukan untuk menghapus satu elektron dari suatu atom dalam keadaan gas untuk membentuk ion positif. Ketika suatu atom kehilangan satu elektron, ia menjadi ion positif karena jumlah proton di inti atom tetap, sementara jumlah elektron berkurang. Energi ionisasi diukur dalam satuan energi per mol atau elektron-volt (eV).
2. Afinitas Elektron
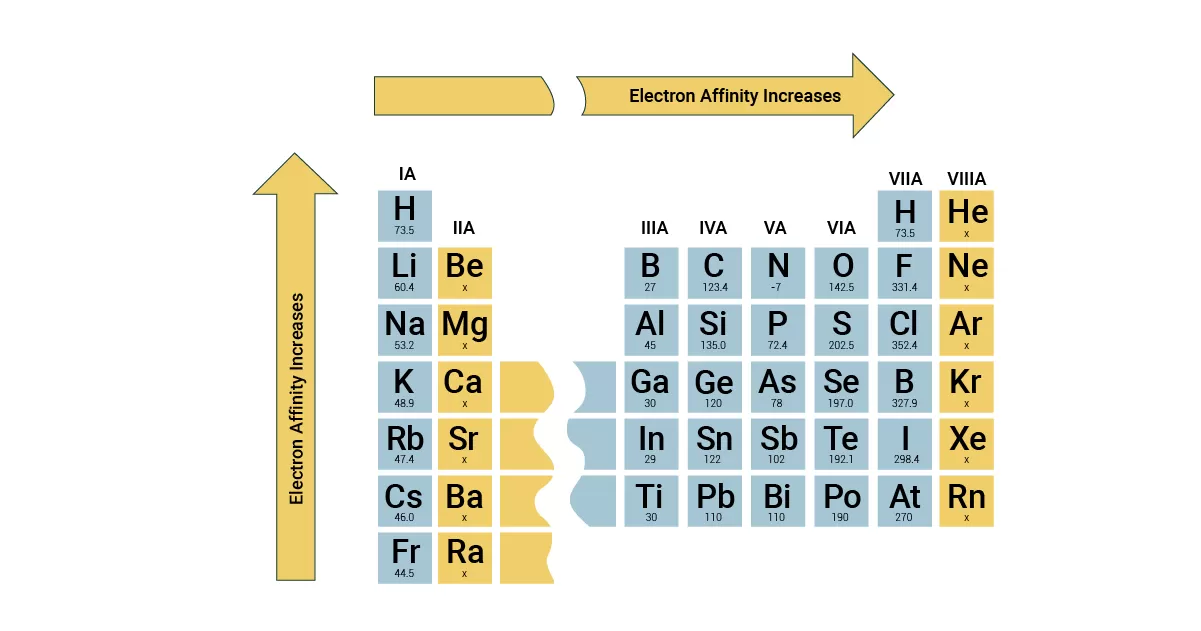
Pengertian afinitas elektron adalah energi yang dilepaskan atau diserap saat satu elektron ditambahkan ke atom dalam keadaan gas untuk membentuk ion negatif. Ketika suatu atom menerima satu elektron, ia menjadi ion negatif (anion) karena jumlah proton di inti atom tetap, sementara jumlah elektron bertambah. Afinitas elektron juga diukur dalam satuan energi per mol atau elektron-volt (eV), namun, seringkali afinitas elektron lebih sering diukur dalam satuan energi negatif karena energi dilepaskan selama proses.
Dengan kata lain, energi ionisasi melibatkan pengeluaran energi untuk melepaskan elektron, sementara afinitas elektron melibatkan penyerapan energi saat menambahkan elektron. Beberapa atom memiliki energi ionisasi yang rendah, yang membuatnya lebih mudah kehilangan elektron, sementara beberapa atom memiliki afinitas elektron yang tinggi, yang berarti mereka cenderung menarik elektron.
Kedua konsep ini sangat relevan dalam pemahaman sifat-sifat kimia dan perilaku reaksi kimia atom dan molekul.