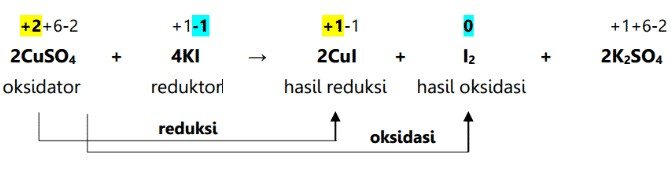
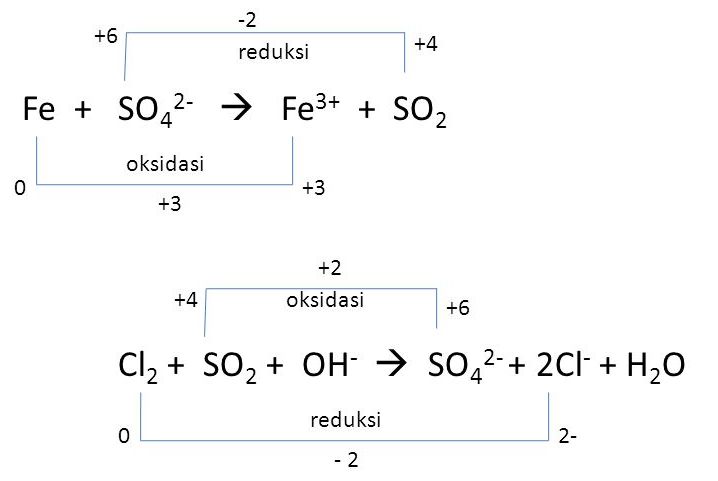
Reaksi redoks berdasarkan perubahan bilangan oksidasi dapat mengalami reaksi reduksi jika suatu atom dalam reaksi redoks tersebut mengalami penurunan bilangan oksidasi dan jika terjadi peningkatan bilangan oksidasi maka atom tersebut mengalami reaksi oksidasi.
Berikut ini adalah contoh reaksi redoks berdasarkan perubahan bilangan oksidasi.
Contoh reaksi redoks yang lain:
- Na(s) + H2O(l) → NaOH(aq) + H2(g)
- Mg(s) + H2S(g) → MgS(s) + H2(g)
- Al(s) + Cl2(g) → AlCl3(g)
- 2Na(s) + H2(g) → 2NaH(g)
- Al(s) + O2(g) → Al2O3(s)
- K(s) + H2O(l) → KOH(aq) + H2(g)
- Ca(s) + Cl2(g) → CaCl2(s)
- H2(g) + Cl2(g) → HCl(g)
- MnO2(s) + 2H2SO4(aq) + 2NaI(aq) → MnSO4(aq) + Na2SO4(aq) + 2H2O(l) + I2(s)
- Zn + 2HCl → ZnCl2 + H2
- Cl2 + SO2 + 2H2O → 2HCl + H2SO4
- CuO + H2 → Cu + H2O
- Cl2 + 2KOH → KCl + KClO + H2O
- 2H2S + SO2 → 3S + 2H2O
- KMnO4 + KI + H2SO4 → MnSO4 + I2 + K2SO4 + H2O
- 2CuSO4 + 4KI → 2K2SO4 + 2CuI2 + I2
- 4Na + O2 → 2NaO
- 2KMnO4 + 16HCl → 2MnCl2 + 2KCl + 5Cl2 + 8H2O
- Ca + F2 → CaF2
- 2Na2S2O3 + HCl → 2S + 2SO2 + 2H2O + NaCl
- Pb + PbO2 + 2H2SO4 → 2PbSO4 + 2H2O
- 6NaOH + 3Cl2 → 5NaCl + NaClO3 + 3H2O
- 2H2 + O2 → 2H2O
- 2CuO + N2 → 2Cu + 2NO
- Fe2O3 + 2Al → Al2O3 + 2Fe