Soal No. 11
Diketahui energi ikatan kJ/mol, rata-rata untuk C – H = 413, C = C = 614, C – C = 348, C ≡ C = 839, H – H = 438. Perubahan ∆H C2H2(g) + H2(g) → C2H4(g) …. kJ
A. -663
B. -1930
C. 663
D. 1930
E. -482
Jawaban: C
Soal No. 12
Bila diketahui energi ikatan rata-rata untuk:
- C – H : +417 kJ/mol
- C = C : +609 kJ/mol
- C – C : 349,02 kJ/mol
- H – H : 437,64 kJ/mol
Maka besarnya perubahan entalpi reaksi adisi C4H8 oleh gas H2 adalah …. kJ/mol
A. -280,56
B. -136,38
C. -28,06
D. 136,38
E. 280,56
Jawaban: B
Soal No. 13
Perubahan entalpi pembentukan gas HCl = -a kJ; energi ikatan H2 dan Cl2 masing-masing b dan c. Besarnya energi ikatan H – Cl pada senyawa adalah …. kJ
A. (a + b + c)
B. (a + ½ b + c)
C. (a + b – c)
D. (½ a + ½ b – c)
E. (½ a + b – c)
Jawaban: A
Soal No. 14
Diketahui energi ikatan rata-rata:
- C = C : +145 kkal
- C – C : +83,1 kkal
- H – H : +104,2 kkal
- C – H : +98,8 kkal
∆H untuk reaksi C2H4 + H2 → C2H6 adalah ….
A. -31,5 kkal
B. +56,6 kkal
C. -56,6 kkal
D. +166,1 kkal
E. -166,1 kkal
Jawaban: A
Soal No. 15
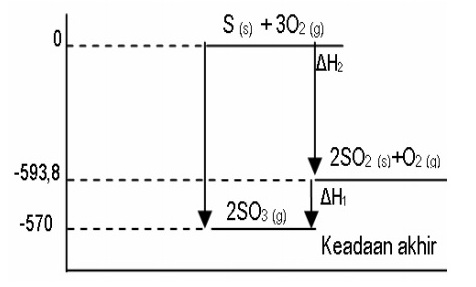
Diagram tahap reaksi pembentukan gas SO3
Berdasarkan diagram tersebut, ∆H2 adalah ….
A. 790,4 kJ
B. 593,8 kJ
C. 196,6 kJ
D. -196,6 kJ
E. -593,8 kJ
Jawaban: E
Soal No. 16
Diagram entalpi tahap-tahap reaksi sebagai berikut:
Dari diagram perubahan entalpi di atas, maka ∆Hf untuk reaksi S(s) + O2(g) → SO2(g) adalah ….
A. 296,9 kJ/mol
B. -296,9 kJ/mol
C. 593,8 kJ/mol
D. -593,8 kJ/mol
E. 987,0 kJ/mol
Jawaban: C
Soal No. 17
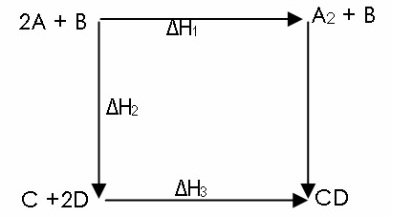
Berdasarkan siklus:
Perubahan entalpi A2B → CD2 adalah ….
A. ∆H1 + ∆H2 + ∆H3
B. -∆H1 – ∆H2 – ∆H3
C. -∆H1 + ∆H2 + ∆H3
D. ∆H1 – ∆H2 – ∆H3
E. ∆H1 + ∆H2 – ∆H3
Jawaban: C
Soal No. 18
Diketahui energi ikatan rata-rata:
- C = C : 146
- C – H : 99
- C – C : 83
- C – C : 79
- H – Cl : 103
Maka perubahan entalpi pada adisi etana dengan asam klorida menurut persamaan:
H2C = CH2 + HCl → CH3 – CH2Cl adalah ….
A. 510 kkal
B. -72,8 kkal
C. -12 kkal
D. 12 kkal
E. 510 kkal
Jawaban: C
Soal No. 19
Sebanyak 50 mL larutan HCl 1M direaksikan dengan 50 mL larutan NaOH 1M. Setelah bereaksi suhu larutan berubah dari 270C menjadi 33,50C. Jika massa jenis larutan = 1gram/mL dan kalor jenis larutan = 4,18 J/g0C maka harga ∆H reaksi adalah ….
A. 1,36 kJ/mol
B. 2,72 kJ/mol
C. 5,43 kJ/mol
D. 8,43 kJ/mol
E. 54,34 kJ/mol
Jawaban: E
Soal No. 20
Apabila 100 mL larutan NaOH 1M direaksikan dengan 100 mL larutan HCl 1 M dalam sebuah bejana, ternyata suhu larutan naik dari 290C menjadi 370C. Jika kalor jenis larutan dianggap sama dengan kalor jenis air = 4,2 J/gr0C, maka perubahan entalpi reaksi
NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(l) adalah …. kJ.
A. -4,50
B. -54,6
C. -67,2
D. -71,4
E. -82,3
Jawaban: C