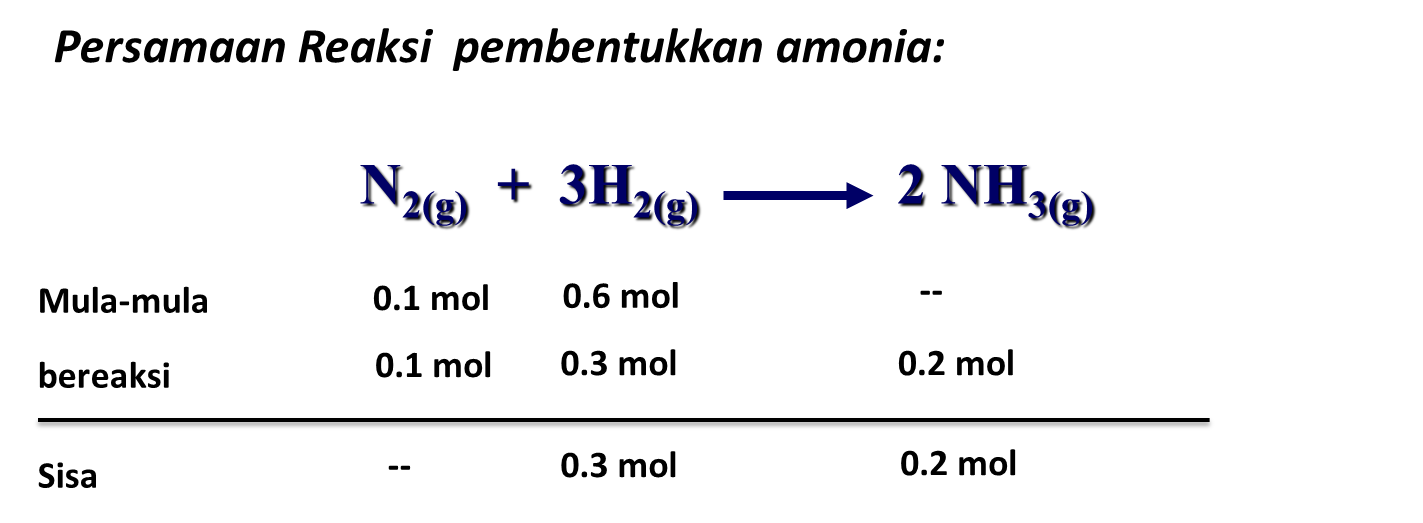Pereaksi pembatas adalah pereaksi yang habis terlebih dahulu sebelum pereaksi yang lainnya habis. Pereaksi sisa adalah pereaksi yang tidak habis bereaksi. Cara menentukan pereaksi pembatas dan peraksi sisa yaitu sebagai berikut langkah-langkahnya:
- Kita tentukan dulu jumlah mol tiap zat pereaksi
- Menyetarakan persamaan reaksi
- Mencari perbandingan mol dan menentukan zat yang habis bereaksi. Zat yang habis bereaksi ini berperan sebagai pereaksi pembatas dan zat yang tidak habis bereaksi berperan sebagai pereaksi sisa.
- Mencari mol zat yang ditanyakan menggunakan mol pereaksi pembatas
- Menyelesaikan pertanyaan yang ditanyakan
Contoh Soal Pereaksi Pembatas dan Pereaksi Sisa:
Contoh No. 1
Sebanyak 28 gram besi (Ar Fe = 56) direaksikan dengan 20 gram belerang (Ar = 32) sesuai persamaan reaksi berikut:
Fe(s) + S(s) → FeS(s)
Tentukan:
- Pereaksi pembatas
- Massa zat yang tersisa
- Massa garam yang terbentuk
Pembahasan:
Langkah 1. Kita tentukan dulu jumlah mol tiap zat pereaksi
n Fe = gr/Ar = 28/56 = 0,5 mol
n S = gr/Ar = 20/32 = 0,625 mol
Langkah 2. Menyetarakan persamaan reaksi
Fe(s) + S(s) → FeS(s)
Langkah 3. Mencari perbandingan mol dan menentukan zat yang habis bereaksi. Zat yang habis bereaksi ini berperan sebagai pereaksi pembatas dan zat yang tidak habis bereaksi berperan sebagai pereaksi sisa.
Perbandingan mol Fe = jumlah mol Fe/koefisien Fe = 0,5/1 = 0,5 mol
Perbandingan mol S = jumlah mol S/koefisien S = 0,625/1 = 0,625 mol
Fe : S = 0,5 : 0,625
Jadi, Fe akan habis bereaksi terlebih dahulu dan berperan sebagai pereaksi pembatas. Sedangkan S berperan sebagai pereaksi sisa (berlebih).
Jumlah mol S sisa = 0,625 – 0,5 = 0,125 mol
n S sisa = gr/Ar
0,125 = gr/32
gr = 0,125 x 32 = 4 gram
Langkah 4. Mencari mol zat yang ditanyakan menggunakan mol pereaksi pembatas
Jumlah mol FeS = (Koefisien FeS/Koefisien Fe) x jumlah mol Fe
Jumlah mol FeS = (1/1) x 0,5 = 0,5 mol
Langkah 5. Menyelesaikan pertanyaan yang ditanyakan
n FeS = gr/Mr
0,5 = gr/88
gr = 0,5 x 88 = 44 gram
Jawaban:
- Pereaksi pembatas = Fe
- Massa zat yang tersisa = 4 gram
- Massa garam yang terbentuk = 44 gram
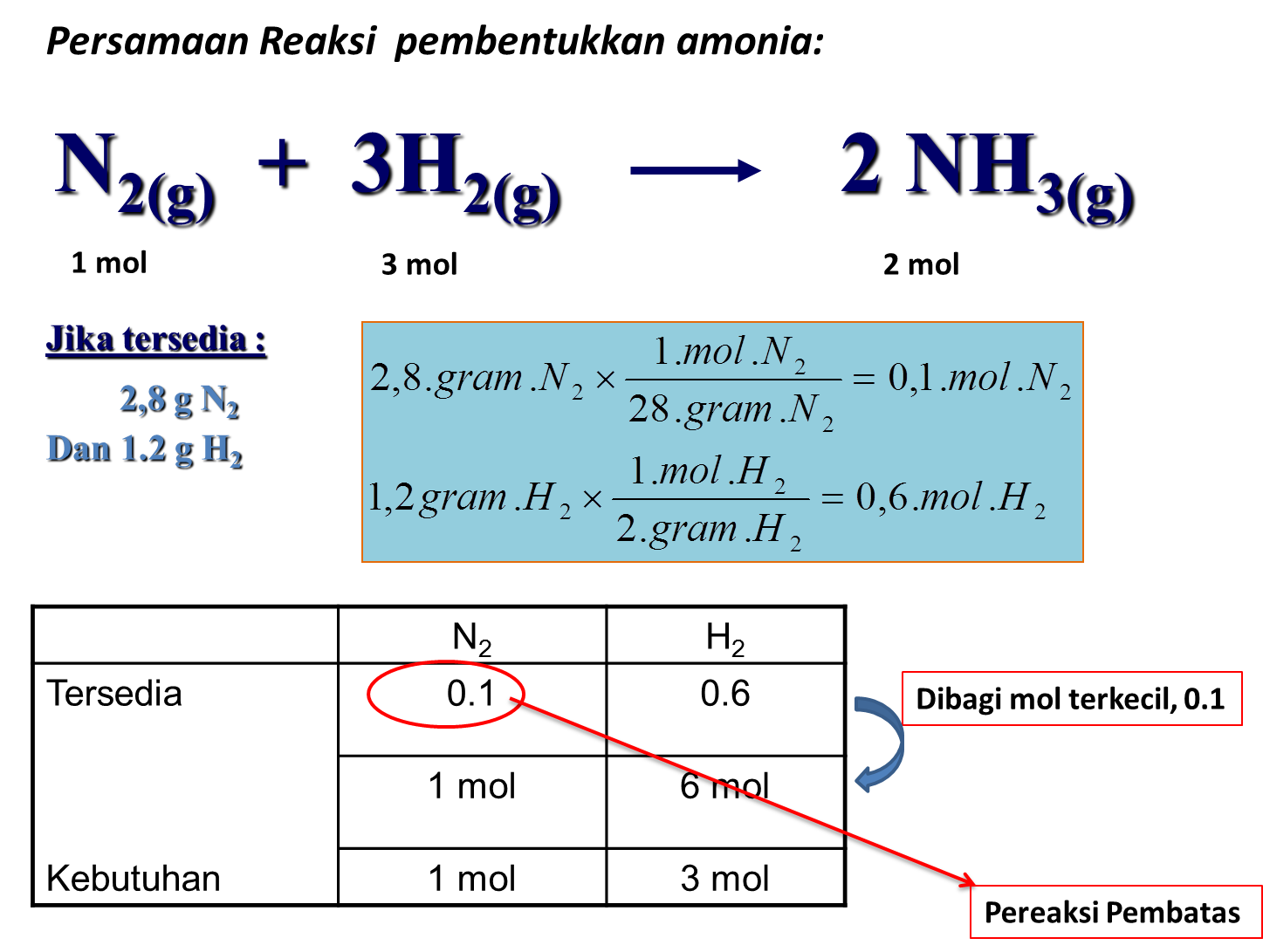
Contoh No. 2
Jadi yang berperan sebagai pereaksi pembatas adalah nitrogen. Gas hidrogen pereaksi berlebih dan amonia yang dihasilkan adalah sebanyak 0,2 mol.