Bentuk molekul merupakan gambaran secara teoritis susunan atom-atom dalam molekul berdasarkan susunan ruang pasangan elektron ikatan dan pasangan elektron bebas atom pusat. Bentuk molekul dapat ditentukan dengan dua cara, yaitu menentukan bentuk molekul berdasarkan teori domain elektron (jumlah pasangan elektron valensi atom pusat) dan teori hibridisasi. Namun, yang akan kita bahas kali ini hanya berdasarkan teori domain elektron saja.
Teori VSEPR
Menurut teori VSEPR (Valence Shell Electron Pair Repulsion) yang berbunyi “pasangan-pasangan elektron akan berusaha saling menjauhi sehingga tolak-menolak antara pasangan elektron menjadi minimum” .
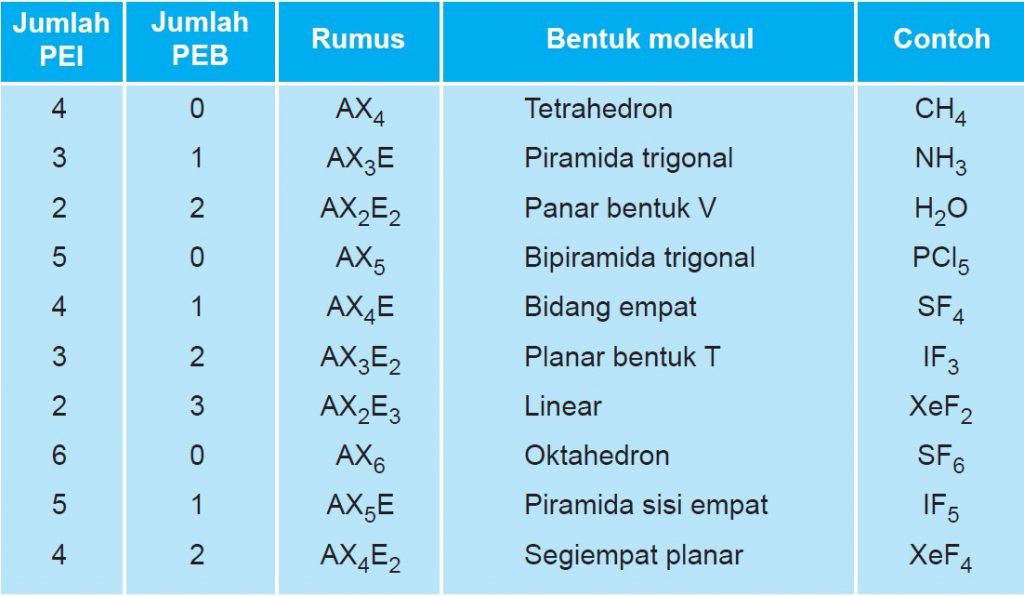
bentuk molekul dapat diramalkan dari jumlah pasangan elektron valensi atom pusat, dan juga posisi pasangan elektron tersebut dalam atom pusat. Jika jumlah elektron dalam domain elektron semakin banyak, maka gaya tolak-menolaknya semakin besar. Berdasarkan kenyataan tersebut dapat diramalkan bentuk molekul dari beberapa senyawa sebagai berikut
Lantas bagaimana cara menentukan bentuk molekul berdasarkan teori doamain elektron? Untuk menentukan bentuk molekul berdasarkan teori domain elektron yang harus kita lakukan yaitu:
- Menuliskan struktur Lewis senyawa yang bersangkutan
- Menentukan jumlah pasangan elektron di sekitar atom pusat (PE)
- Menentukan jumlah pasangan elektron ikatan (PEI)
- Menentukan jumlah pasangan elektron bebas (PEB)
- Selanjutnya tinggal menentukan rumus bentuk molekulnya
- Jika kita belum yakin dengan hasil yang kita dapatkan, maka bandingkan hasilnya dengan tabel di atas.
Bagaimana? mudah bukan! selanjutnya, biar tambah pinter, mari kita kerjakan contoh soal berikut ini.
Contoh soal:
Bagaimana bentuk molekul CO2 berdasarkan teori domain elektron?
Jawaban
1. Tulis struktur Lewis CO2 (jumlah elektron terluar C : 4 dan O : 6)
2. Dari struktur O=C=O itu diperoleh
- Jumlah elektron di sekitar atom pusat = 2
- Jumlah elektron ikatan = 2
- Jumlah elektron bebas = 0
3. Jadi, rumus yang diperoleh AX2
4. Berdasarkan tabel di atas, rumus AX2 merupakan bentuk molekul linear
Jadi, bentuk molekul CO2 adalah linear.