A. Pengertian Orde Reaksi
Orde reaksi menyatakan besarnya pengaruh konsentrasi pereaksi pada laju reaksi.
B. Rumus Orde Reaksi
Beberapa orde reaksi yang umum terdapat dalam persamaan reaksi kimia beserta rumusnya adalah sebagai berikut.
1. Reaksi Orde Nol (0)
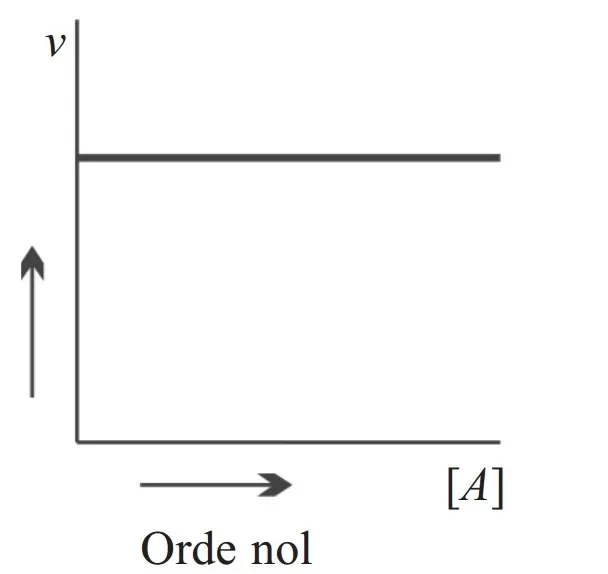
Suatu reaksi kimia dikatakan mempunyai orde reaksi nol, jika besarnya laju reaksi tersebut tidak dipengaruhi oleh konsentrasi pereaksi. Artinya, seberapapun peningkatakn konsentrasi pereaksi tidak akan mempengaruhi besarnya laju reaksi.
Rumus laju reaksi orde nol secara matematis dituliskan sebagai berikut.
r = k [A]0
2. Reaksi Orde Satu (1)
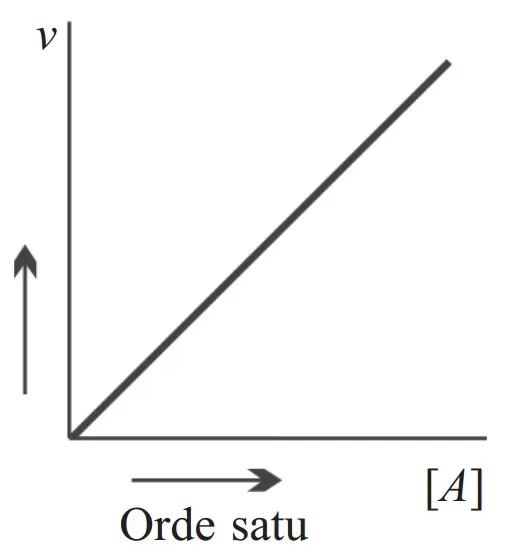
Suatu reaksi kimia dikatakan mempunyai orde satu, apabila besarnya laju reaksi berbanding lurus dengan besarnya konsentrasi pereaksi. Artinya, jika konsentrasi pereaksi dinaikkan dua kali semula, maka laju reaksi juga akan meningkat besarnya sebanyak (2)¹ atau 2 kali semula juga.
Rumus laju reaksi orde satu secara matematis dituliskan sebagai berikut.
r = k [A]
3. Reaksi Orde Dua (2)
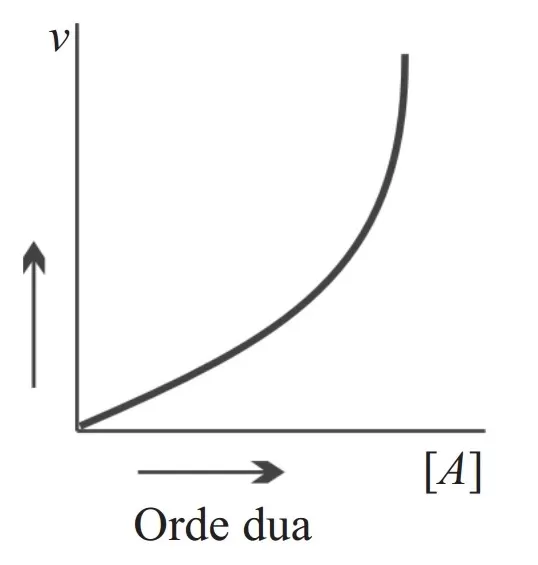
Suatu reaksi dikatakan mempunyai orde dua, apabila besarnya laju reaksi merupakan pangkat dua dari peningkatan konsentrasi pereaksinya. Artinya, jika konsentrasi pereaksi dinaikkan 2 kali semula, maka laju reaksi akan meningkat sebesar (2)² atau 4 kali semula.
Apabila konsentrasi pereaksi dinakkan 3 kali semula, maka laju reaksi akan menjadi (3)² atau 9 kali semula.
Rumus laju reaksi orde dua secara matematis dituliskan sebagai berikut.
r = k [A]2
4. Reaksi Orde Negatif
Suatu reaksi kimia dikatakan mempunyai orde negatif, apabila besarnya laju reaksi berbanding terbalik dengan konsentrasi pereaksi. Artinya, apabila konsentrasi pereaksi dinaikkan atau diperbesar, maka laju reaksi akan menjadi lebih kecil.