Perkembangan konsep reaksi reduksi oksidasi (redoks) terdiri dari tiga konsep yaitu:
- Reaksi reduksi oksidasi sebagai pengikatan dan pelepasan oksigen.
- Reaksi reduksi oksidasi sebagai pelepasan dan penerimaan elektron.
- Reaksi reduksi oksidasi sebagai pertambahan dan pengurangan bilangan oksidasi.
Secara lebih terperinci, mari simak ulasan berikut ini.
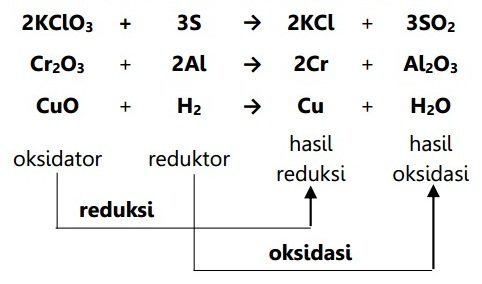
1. Konsep Reaksi Redoks berdasarkan Pengikatan dan Pelepasan Oksigen
Berdasarkan konsep ini,
- Reduksi adalah reaksi dimana suatu zat berupa oksida direaksikan dengan zat yang menarik oksigen sehingga oksida tersebut kehilangan oksigen.
- Oksidasi adalah reaksi dimana suatu zat direaksikan dengan sumber oksigen sehingga berikatan dengan oksigen tersebut membentuk oksida.
- Oksidator adalah sumber oksigen.
- Reduktor adalah penarik oksigen.
Contoh reaksi redoks berdasarkan pengikatan dan pelepasan oksigen:
Kelemahan konsep ini yaitu:
- Konsepnya terlalu sempit.
- Tidak seluruh reaksi baik itu oksidasi maupun reduksi terjaddi secara redoks.
- Tidak seluruh reaksi oksidasi melibatkan reaksi reduksi.
- Tidak seluruh reaksi reduksi melibatkan reaksi oksidasi.
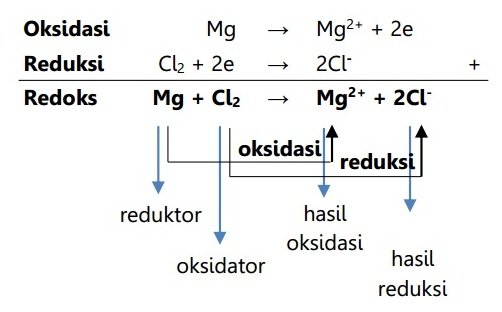
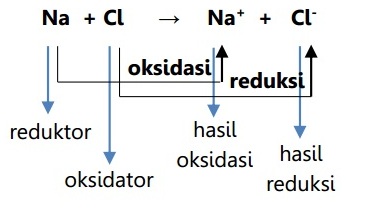
2. Konsep Reaksi Redoks berdasarkan Pelepasan dan Penerimaan Elektron
Berdasarkan konsep ini,
- Reduksi adalah reaksi yang disertai dengan penerimaan elektron.
- Oksidasi adalah reaksi yang disertai dengan pelepasan elektron.
- Oksidator adalah penerima elektron.
- Reduktor adalah pemberi elektron.
Contoh reaksi redoks berdasarkan pelepasan dan penerimaan elektron:
3. Konsep Reaksi Redoks berdasarkan Pertambahan dan Pengurangan Bilangan Oksidasi
Berdasarkan konsep ini,
- Reduksi adalah reaksi yang mengalami penurunan bilangan oksidasi.
- Oksidasi adalah reaksi yang mengalami pertambahan bilangan oksidasi.
- Oksidator adalah zat yang mengalami penurunan bilangan oksidasi.
- Reduktor adalah zat yang mengalami pertambahan bilangan oksidasi.
Contoh reaksi redoks berdasarkan konsep pertambahan dan pengurangan bilangan oksidasi: