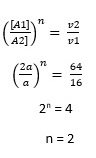Soal UNBK Kimia 2018 dan Pembahasannya No. 11-15
Soal UN Kimia No. 11
Perhatikan tabel persamaan reaksi hidrolisis garam berikut ini!
| No. | Rumus Garam | Reaksi Hidrolisis | Perkiraan pH | Sifat |
| 1 | CH3COONa | CH3COO–(aq) + H2O(l) ⇌ CH3COOH + OH–(aq) | >7 | Basa |
| 2 | CaSO3 | SO3–(aq) + H2O(l) ⇌ HSO3–(aq) + OH–(aq) | <7 | Basa |
| 3 | (NH4)2SO4 | NH4+(aq) + H2O(l) ⇌ NH3(aq)+ H3O+(aq) | <7 | Asam |
| 4 | (NH4)3PO4 | PO4+(aq) + H2O(l) ⇌ HPO42-(aq) + H–(aq)
NH4+(aq) + H2O(l) ⇌ NH3(aq) + H3O+(aq) |
>7 | Basa |
Pasangan data garam terhidrolisis yang tepat adalah ….
A. (1) dan (2)
B. (1) dan (3)
C. (1) dan (4)
D. (2) dan (3)
E. (2) dan (4)
Jawaban: B
Pembahasan:
Hidrolisis garam adalah reaksi penguraian garam dalam air. Apabila garam tersebut membentuk ion H+ atau H3O+maka garam tersebut bersifat asam. Sedangkan jika garam tersebut membentuk ion OH−maka garam tersebut bersifat basa.
Soal UN Kimia No. 12
Diketahui data beberapa indikator dan trayek pH.
| Indikator | Metil Jingga | Bromtimol Biru | Fenolftalein |
| Trayek pH | 3,1 – 4,40 | 6,0 – 7,6 | 8,3 – 10,0 |
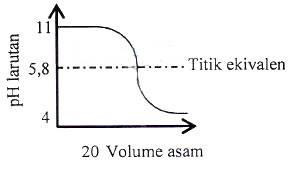
Berikut ini adalah kurva titrasi asam-basa.
Pasangan asam-basa/basa-asam dan indikator yang digunakan berturut-turut adalah ….
A. KOH – CH3COOH – fenolftalein
B. KOH – HCl – fenolftalein
C. CH3NH3 – HCl – metil jingga
D. NH4OH – CH3COOH – metil jingga
E. NaOH – HCl – fenolftalein
Jawaban: C
Pembahasan:
- Titrasi terjadi antara asam kuat dan basa lemah. Di antara opsi jawaban, yang termasuk basa lemah dan asam kuat adalah CH3NH3 – HCl.
- Titik ekuivalen masuk dalam trayek asam lemah (3 – 6). Sehingga indikator yang tepat adalah metil jingga.
Soal UN Kimia No. 13
Diketahui Ksp Mg(OH)2 = 6 × 10−12. Dua buah larutan dicampur dengan komposisi sebagai berikut:
| No. | Mg(NO3)2 | KOH |
| 1 | 200 mL, 10-3 M | 200 mL, 10-5 M |
| 2 | 100 mL, 10-4 M | 100 mL, 10-3 M |
| 3 | 400 mL, 10-5 M | 400 mL, 10-4 M |
| 4 | 250 mL, 10-3 M | 250 mL, 10-3 M |
| 5 | 500 mL, 10-5 M | 500 mL, 10-5 M |
Pasangan campuran yang menghasilkan endapan Mg(OH)2 ditunjukkan pada nomor ….
A. (1) dan (4) karena harga Qc < Ksp
B. (1) dan (5) karena harga Qc > Ksp
C. (2) dan (3) karena harga Qc < Ksp
D. (2) dan (4) karena harga Qc > Ksp
E. (3) dan (5) karena harga Qc < Ksp
Jawaban: D
Pembahasan:
| No. | [Mg2+] | [OH−] | Qc = [Mg2+] [OH−]2 | Ksp | Ket |
| (1) | 10−3 | 10−5 | 10−13 | 6 × 10−12 | Qc < Ksp |
| (2) | 10−4 | 10−3 | 10−10 | Qc > Ksp | |
| (3) | 10−5 | 10−4 | 10−13 | Qc < Ksp | |
| (4) | 10−3 | 10−3 | 10−9 | Qc > Ksp | |
| (5) | 10−5 | 10−5 | 10−15 | Qc < Ksp |
Ingat kembali!
- Qc < Ksp : belum jenuh
- Qc = Ksp : tepat jenuh
- Qc > Ksp : lewat jenuh (terdapat endapan)
Jadi, pasangan campuran yang menghasilkan endapan Mg(OH)2 ditunjukkan pada nomor 2 dan 4.
Soal UN Kimia No. 14
Jika kita memasukkan bongkahan batu kapur ke dalam air, akan terjadi gelembung-gelembung gas dan wadah akan terasa panas.
Pernyataan yang benar dari data percobaan tersebut adalah …
A. Reaksi tersebut merupakan reaksi eksoterm karena sistem menyerap kalor dari lingkungan.
B. Reaksi tersebut merupakan reaksi endoterm karena lingkungan menyerap kalor dari sistem.
C. Reaksi tersebut merupakan reaksi eksoterm karena sistem melepas kalor ke lingkungan.
D. Reaksi tersebut merupakan reaksi endoterm karena lingkungan menerima kalor dari sistem.
E. Reaksi tersebut merupakan reaksi eksoterm karena lingkungan melepas kalor ke sistem.
Jawaban: C
Soal UN Kimia No. 15
Diketahui data percobaan reaksi 2A + B2 → 2AB.
| Percobaan | [A] M | [B] M | Waktu | v (m/detik) |
| (1) | a | b | 288 s | 16 |
| (2) | 2a | b | 72 s | 64 |
| (3) | 3a | 2b | 16 s | 72 |
Jawaban: C
Pembahasan:
persamaan laju reaksinya:
v = k [A]2 [B]m
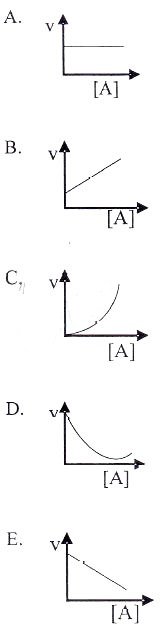
v ~ [A]2
Itu artinya, grafik v – [A] adalah grafik kuadrat atau parabola.