Soal UN Kimia 2019 No. 12
Perhatikan dua notasi atom unsur berikut!
12X6 dan 1Y1
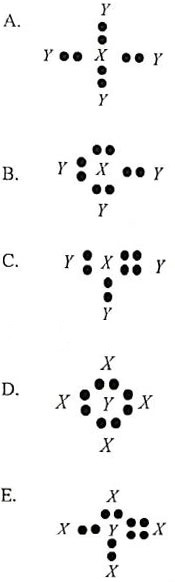
Bila unsur X dan Y berikatan, struktur Lewis molekul senyawa yang terbentuk adalah ….
Jawaban: A
Pembahasan:
6X = 2, 4
1Y = 1
Itu artinya, apabila atom X berikatan dengan atom Y akan membentuk senyawa XY4. Struktur Lewis dari senyawa XY4 ditunjukkan seperti pada pilihan A.
Soal UN Kimia 2018 No. 4
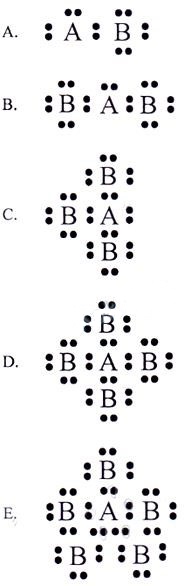
Jika unsur A (nomor atom 7) dan B (nomor atom 17) berikatan, struktur Lewis yang benar adalah ….
Jawaban: C
Pembahasan:
7A = 2, 5
17B = 2, 8, 7
Unsur A mempunyai 5 elektron valensi sehingga membutuhkan 3 elektron lagi agar terpenuhi kaidah oktet. Sedangkan unsur B mempunyai 7 elektron valensi sehingga membutuhkan 1 elektron lagi biar memenuhi kaidah oktet. Dengan demikian, senyawa yang terbentuk adalah AB3.
Soal UN Kimia 2017 No. 7
Gambar struktur Lewis senyawa SO2 yang paling tepat adalah … (nomor atom S = 16; O = 8).
Jawaban: B
Pembahasan:
Untuk dapat mengetahui struktur lewis senyawa SO2, kita harus menentukan elektron valensi dari S dan O, yaitu:
16S = 2 8 6
8O = 2 6
seperti kita lihat, kedua unsur sama-sama memerlukan 2 elektron lagi untuk stabil. Sehingga, Struktur Lewisnya:
Soal UN Kimia 2016 No. 3
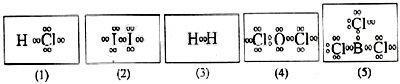
Perhatikan gambar struktur Lewis beberapa senyawa berikut!
Senyawa yang tidak mengikuti kaidah oktet atau duplet adalah ….
A. (1)
B. (2)
C. (3)
D. (4)
E. (5)
Jawaban: E
Pembahasan:
BCl3 tidak mengikuti kaidah oktet atau duplet karena pada atom B hanya terdapat 6 elektron.
Soal UN Kimia 2015 No. 1
Unsur M dan N memiliki konfigurasi elektron sebagai berikut:
M : [Ar] 4s2
N : [Ne] 3s2 3p5
Apabila M dan N berikatan, rumus senyawa yang terbentuk adalah ….
A. MN
B. MN2
C. MN3
D. M2N
E. M3N
Jawaban: B
Pembahasan:
M : [Ar] 4s2 → M2+
N : [Ne] 3s2 3p5 → N–
M2+ + 2N– → MN2
Soal UN Kimia 2014 No. 1
Berikut ini beberapa senyawa kovalen:
- CH4
- NH3
- PCl5
- PCl3
- CO2
(Nomor atom: C = 6; H = 1; N = 7; P = 15; Cl = 17; dan O = 8). Senyawa kovalen yang mengalami penyimpangan kaidah oktet dalam struktur Lewisnya adalah ….
A. (1)
B. (2)
C. (3)
D. (4)
E. (5)
Jawaban: C
Pembahasan:
1. CH4
6C = 2, 4 (kekurangan 4 elektron)
1H = 1 (kekurangan 1 elektron)
CH3 = 4 + 1 × 4 = 8 [oktet].
2. NH3
7N = 2, 5 (kekurangan 3 elektron)
1H = 1 (kekurangan 1 elektron)
NH3 = 5 + 1 × 3 = 8 [oktet].
3. PCl5
15P = 2, 8, 5 (kekurangan 3 elektron)
17Cl = 2, 8, 7 (kekurangan 1 elektron)
PCl3 = 5 + 1 × 5 = 10 [bukan oktet].
4. PCl3
15P = 2, 8, 5 (kekurangan 3 elektron)
17Cl = 2, 8, 7 (kekurangan 1 elektron)
PCl3 = 5 + 1 × 3 = 8 [oktet].
5. CO2
6C = 2, 4 (kekurangan 4 elektron)
8O = 2, 6 (kekurangan 2 elektron)
CO2 = 4 + 2 × 2 = 8 [oktet].